
|
| ļ¬®ņĀü ļ░Å ļ▓öņ£ä Aims and Scope |
| ņĀĆļäÉ ņĀĢļ│┤ About the Journal |
| ĒÄĖņ¦æņ£äņøÉĒÜī Editorial Board |
| Open Access |
| ĒÄĖņ¦æĻĄŁ Editorial Office |


|
| ļ¬®ņĀü ļ░Å ļ▓öņ£ä Aims and Scope |
| ņĀĆļäÉ ņĀĢļ│┤ About the Journal |
| ĒÄĖņ¦æņ£äņøÉĒÜī Editorial Board |
| Open Access |
| ĒÄĖņ¦æĻĄŁ Editorial Office |

AbstractElectrodialysis was used to develop a highly efficient process for concentrating and recovering Li from the Li-containing waste solution that is generated after recovering Co and Ni from a leach solution of waste cathode materials of Li ion batteries. The optimum conditions were investigated by comparing the concentration of Li in the concentrated solution, water recovery rate, energy consumption and average flow rate. Limiting current density was also checked. The results showed that the concentration ratio of Li was enhanced up to 133.33% at an applied voltage of 10 V and volume ratio(VD/VC) of 4/1. In order to investigate the concentration ratio of Li based on large volume ratio, the total volume of the Li-containing solution was fixed, and the volume ratio of the dilute solution to the concentrate solution was adjusted to 1/1 to 10/1. The concentration ratio of lithium was increased in the initial stage and then decreased due to the osmotic phenomenon. Finally, an the analysis of the experimental results, including concentration ratio, average flux, and energy consumption, determined that the volume ratio(VD/VC) of 3/1 at 10 V of applied voltage was most efficient and the concentrate ratio of Li increased up to 160.61%.
1. ņä£ ļĪĀļ”¼ĒŖ¼ņØĆ ņĀäĻĖ░ņ×ÉļÅÖņ░©, ņŖżļ¦łĒŖĖĒÅ░, ļģĖĒŖĖļČü ļō▒ņØś ņØ┤ņ░©ņĀäņ¦Ć ļśÉļŖö ņŚÉļäłņ¦ĆņĀĆņןņןņ╣ś(Energy Storage System, ESS) ļō▒ņŚÉ ĒĢĄņŗ¼ļČĆĒÆłņ£╝ļĪ£ ņō░ņØ┤ļŖö ņ×ÉņøÉņ£╝ļĪ£ ļ”¼ĒŖ¼ņØ┤ņś©ļ░░Ēä░ļ”¼ņŚÉ ļīĆĒĢ£ ņŚ░ĻĄ¼Ļ░Ć ĒÖ£ļ░£ĒĢśĻ▓ī ņ¦äĒ¢ēļÉśĻ│Ā ņ׳ņ£╝ļ®░ ņĀäĻĖ░ņ×ÉļÅÖņ░© ņŗ£ņן ņä▒ņןņŚÉ ļö░ļźĖ ļ”¼ĒŖ¼ņØ┤ņś©ļ░░Ēä░ļ”¼ņØś ņłśņÜö ņ”ØĻ░Ć ļ░Å Ļ│ĄĻĖēļČĆņĪ▒ ļō▒ņ£╝ļĪ£ ņØĖĒĢ┤ 2015ļģä ņØ┤Ēøä Ļ░ĆĻ▓®ņØ┤ 3.5ļ░░ ņØ┤ņāü ĻĖēļō▒ĒĢśņśĆļŗż [1,2]. ņÜ░ļ”¼ļéśļØ╝ļŖö ļ”¼ĒŖ¼ ļČĆņĪ┤ļ¤ēņØ┤ Ļ▒░ņØś ņŚåĻĖ░ ļĢīļ¼ĖņŚÉ ņĀäļ¤ē ņłśņ×ģņŚÉ ņØśņĪ┤ĒĢśĻ│Ā ņ׳ļŖö ņŗżņĀĢņØ┤ļ®░, ņäĖĻ│äņĀüņ£╝ļĪ£ ņłśņÜöļīĆļ╣ä Ļ│ĄĻĖēņØ┤ ļČĆņĪ▒ĒĢ┤ņ¦Ćļ®┤ ĻĄŁļé┤ ņé░ņŚģņŚÉ Ēü░ ĒāĆĻ▓®ņØä ņŻ╝Ļ▓ī ļÉ£ļŗż. ļö░ļØ╝ņä£ ĻĄŁļé┤ ņĢłņĀĢņĀüņØĖ ņłśĻĖē ļ░®ļ▓ĢņØ┤ ņĀłņŗżĒĢ£ ņŗżņĀĢņØ┤ļŗż.
ĻĖłņåŹļ”¼ĒŖ¼ņØĆ Ļ┤æņäØļ│┤ļŗż ņŚ╝ņłśņŚÉ ņĢĮ 2ļ░░ ļŹö ļ¦ÄņØ┤ ņĪ┤ņ×¼ĒĢ£ļŗż. ļö░ļØ╝ņä£ ņŚ╝ņłśņŚÉņä£ņØś ļ”¼ĒŖ¼ ĒÜīņłśņŚÉ ļīĆĒĢ£ ņŚ░ĻĄ¼Ļ░Ć ĒÖ£ļ░£Ē׳ ņ¦äĒ¢ēļÉśĻ│Ā ņ׳ņ£╝ļéś ņŚ╝ņłś ļé┤ Mg2+, Ca2+Ļ│╝ Ļ░ÖņØĆ ļČłņł£ļ¼╝ņØ┤ ļ¦ÄņĢä ņĀĢņĀ£Ļ│ĄņĀĢņØ┤ ņÜöĻĄ¼ļÉśĻ│Ā, ļ”¼ĒŖ¼ņØś ļåŹļÅäĻ░Ć ļé«ņĢä ļ¦ÄņØĆ ņ¢æņØś ņŚ╝ņłśļź╝ ļåŹņČĢĒĢ┤ņĢ╝ĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ēņØ┤ ļåÆĻ│Ā ņןņŗ£Ļ░äņØś Ļ│ĄņĀĢņØ┤ ņåīņÜöļÉśņ¢┤ Ļ░ĆĻ▓® Ļ▓Įņ¤üļĀź ļśÉĒĢ£ ļé«ņØĆ ĒÄĖņØ┤ļŗż [3-9]. ļśÉĒĢ£ ņé░ņŚģņŚÉņä£ ļ”¼ĒŖ¼ņØ┤ ņé¼ņÜ®ļÉĀ ļĢī ņŻ╝ļĪ£ Ēāäņé░ļ”¼ĒŖ¼ņØ┤ ņøÉļŻīĻ░Ć ļÉśļ®░ ņÜ®ņĢĪ ļé┤ ļ”¼ĒŖ¼ņØä Ēāäņé░ļ”¼ĒŖ¼ņ£╝ļĪ£ ĒÜīņłśĒĢśĻĖ░ ņ£äĒĢ┤ņäĀ ļåŹļÅäĻ░Ć ņØ╝ņĀĢ ņłśņżĆ ņØ┤ņāüņØ┤ņ¢┤ņĢ╝ ĒĢ£ļŗż [10]. ļö░ļØ╝ņä£ ņŚ╝ņłśļ│┤ļŗż ļ”¼ĒŖ¼ņØś ĒĢ©ņ£Āļ¤ēņØ┤ ļåÆĻ│Ā ļČłņł£ļ¼╝ņØ┤ ņĀüņØĆ ļ”¼ĒŖ¼ņØ┤ņś©ļ░░Ēä░ļ”¼ ņ£ĀĻ░ĆĻĖłņåŹ ņČöņČ£ Ēøä ņŚ¼ņĢĪ, ņ”ē ļ”¼ĒŖ¼ĒĢ©ņ£Ā ņøÉļŻīņÜ®ņĢĪņØä ņé¼ņÜ®ĒĢśņŚ¼ ļ”¼ĒŖ¼ņØä ĒÜ©Ļ│╝ņĀüņ£╝ļĪ£ ņ×¼ ņ×ÉņøÉĒÖö ĒĢĀ ņłś ņ׳ļŖö ĻĖ░ņłĀņØä Ļ░£ļ░£ĒĢśĻ│Āņ×É ĒĢśņśĆļŗż.
ņØ╝ļ░śņĀüņ£╝ļĪ£ ņŚ╝ņłś ļō▒ ļ”¼ĒŖ¼ĒĢ©ņ£Ā ņÜ®ņĢĪņŚÉņä£ ļ”¼ĒŖ¼ņØä ĒÜīņłśĒĢśļŖö Ļ│ĄņĀĢņ£╝ļĪ£ļŖö ņ”Øļ░£ļåŹņČĢļ▓ĢņØ┤ ņāüņÜ®ĒÖöļÉśņ¢┤ ņ׳ņ£╝ļéś Ļ│ĀņŚÉļäłņ¦Ć Ļ│ĄņĀĢņØ┤ļ®┤ņä£ ĒÜīņłśņ£©ņØ┤ ļé«ļŗżļŖö ļŗ©ņĀÉņØ┤ ņ׳ļŗż. ņĄ£ĻĘ╝ņŚÉ Ļ░£ļ░£ļÉ£ ņÜ®ļ¦żņČöņČ£ļ▓ĢņØś Ļ▓ĮņÜ░ļŖö ļ”¼ĒŖ¼ņØś ļåŹļÅäĻ░Ć 1.0 g/L ņØ┤ņāüņŚÉņä£ ĒÜ©Ļ│╝ņĀüņØ┤Ļ│Ā, ņČöņČ£ņĀ£ ņé¼ņÜ®ņŚÉ ņØśĒĢ£ Ļ│ĄņĀĢļ╣äņÜ® ņ”ØĻ░ĆņÖĆ ņ£ĀĻĖ░ņāüņØś ņé¼ņÜ®ņ£╝ļĪ£ ĒÖśĻ▓ĮņśżņŚ╝ ļ¼ĖņĀ£Ļ░Ć ļ░£ņāØļÉ£ļŗż [11-15]. ņĀäĻĖ░Ēł¼ņäØ(electrodialysis)ļ▓ĢņØĆ ņĀäĻĖ░ņן ļé┤ņŚÉņä£ ņØ┤ņś©ĻĄÉĒÖśļ¦ēņØä ĒåĄĒĢ┤ ņØ┤ņś©ņØä ņäĀĒāØņĀüņ£╝ļĪ£ ĒåĄĻ│╝ņŗ£ņ╝£ ļ¬®Ēæ£ņä▒ļČäņØś ļåŹņČĢ ļ░Å ļČłņł£ļ¼╝ ļČäļ”¼ņŚÉ ņŻ╝ļĪ£ ņō░ņØ┤ļŖö Ļ│ĄņĀĢņ£╝ļĪ£ ņÜ┤ņĀä ļÅäņżæņŚÉ ļČĆņé░ļ¼╝ņØ┤ Ļ▒░ņØś ļ░£ņāØĒĢśņ¦Ć ņĢŖĻ│Ā ņČöĻ░ĆņĀüņ£╝ļĪ£ ņ×¼ņé¼ņÜ®ņØä ņ£äĒĢ£ ĒÖöĒĢÖņĀü ņ▓śļ”¼ļź╝ ĒĢśņ¦Ć ņĢŖņĢäļÅä ļÉśļŖö ĒÖśĻ▓Į ņ╣£ĒÖöņĀü Ļ│ĄņĀĢņØ┤ļŗż. ļśÉĒĢ£ ņĀäĻĖ░ņŚÉļäłņ¦Ć ņÖĖņØś ņČöĻ░ĆņĀüņØĖ ņŚÉļäłņ¦Ć ļ│ĆĒÖśņØ┤ ņÜöĻĄ¼ļÉśņ¦Ć ņĢŖĻĖ░ ļĢīļ¼ĖņŚÉ ņŚÉļäłņ¦Ć ĒÜ©ņ£© ņĖĪļ®┤ņŚÉņä£ļÅä ņןņĀÉņØä Ļ░Ćņ¦ĆĻ│Ā ņ׳ņ¢┤ ļ»Ėļלņ¦ĆĒ¢źņĀüņØĖ ĻĖ░ņłĀļĪ£ Ļ░üĻ┤æļ░øĻ│Ā ņ׳ļŗż. ļö░ļØ╝ņä£ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņĀäĻĖ░Ēł¼ņäØļ▓ĢņŚÉ ņØśĒĢ£ ļ”¼ĒŖ¼ņØś ļåŹņČĢņŚÉ ļīĆĒĢ£ ĻĖ░ņ┤ł ņŚ░ĻĄ¼ļź╝ ņ¦äĒ¢ēĒĢśņśĆļŗż.
2. ņØ┤ļĪĀņĀü ļ░░Ļ▓ĮņĀäĻĖ░Ēł¼ņäØņØĆ ņ¢æĻĘ╣Ļ│╝ ņØīĻĘ╣ ņé¼ņØ┤ņØś ņĀäņ£äņ░©ņŚÉ ņØśĒĢśņŚ¼ ņ¢æņØ┤ņś©ņØĆ ņØīĻĘ╣ņ£╝ļĪ£ ņØīņØ┤ņś©ņØĆ ņ¢æĻĘ╣ņ£╝ļĪ£ ņØ┤ļÅÖĒĢśĻ▓ī ļÉśĻ│Ā ļæÉ ņĀäĻĘ╣ ņé¼ņØ┤ņŚÉ ņ¢æņØ┤ņś© ĻĄÉĒÖśļ¦ē ļśÉļŖö ņØīņØ┤ņś© ĻĄÉĒÖśļ¦ēņØä ņäżņ╣śĒĢśļ®┤ ņØ┤ņś©ņØ┤ ņäĀĒāØņĀüņ£╝ļĪ£ ņØ┤ļÅÖļÉśņ¢┤ ņØ┤ņś©ņØś ļåŹņČĢĻ│╝ ļČäļ”¼ ĒÜ©Ļ│╝ļź╝ ņ¢╗ņØä ņłś ņ׳ļŗż. ņĀäĻĖ░Ēł¼ņäØ Ļ│ĄņĀĢņŚÉ ņØśĒĢ£ ļ”¼ĒŖ¼ņØś ļåŹņČĢņŚÉ ļīĆĒĢ£ ļ¬©ņŗØļÅäļź╝ ĻĘĖļ”╝ 1ņŚÉ ļéśĒāĆļé┤ņŚłļŗż. ņĀäĻĖ░Ēł¼ņäØ Ļ│ĄņĀĢ ņŗ£ Ļ│ĀļĀżĒĢ┤ņĢ╝ ĒĢĀ ņĀÉņØ┤ ļæÉ Ļ░Ćņ¦Ć ņ׳ļŗż. ĻĘĖ ņżæ ĒĢśļéśļŖö ĒĢ£Ļ│äņĀäļźśļ░ĆļÅä(limiting current density)ļĪ£ ņĀäņĢĢņØä ņŚ░ņåŹņĀüņ£╝ļĪ£ ņ”ØĻ░Ćņŗ£Ēé¼ ļĢī ņĀäļźśĻ░Æ ļśÉĒĢ£ ņ”ØĻ░ĆĒĢśļŗżĻ░Ć ļŹö ņØ┤ņāü ņ”ØĻ░ĆĒĢśņ¦Ć ņĢŖļŖö ĻĄ¼Ļ░äņØ┤ ļ░£ņāØĒĢśļŖö ĒśäņāüņØä ļ¦ÉĒĢśļ®░, ņØ┤ņś©ĻĄÉĒÖśļ¦ē Ļ│äļ®┤Ļ│╝ ņÜ®ņĢĪ ņé¼ņØ┤ņØś ļåŹļÅäļČäĻĘ╣ņŚÉ ņØśĒĢ┤ ļéśĒāĆļé£ļŗż. ĒĢ£Ļ│äņĀäļźś ņØ┤ņāüņØś ņĀäļźśĻ░Ć ņØĖĻ░ĆļÉśļ®┤ ļ¼╝(H2O)ņØ┤ ļČäĒĢ┤ļÉśņ¢┤ ņĢīņ╣╝ļ”¼ ņÜ®ņĢĪņØ┤ ļÉśņ¢┤ ļČłņł£ļ¼╝ņØĖ Mg2+, Ca2+Ļ░Ć ņłśņé░ĒÖöļ¼╝ņØä ĒśĢņä▒ĒĢśĻ│Ā ņ╣©ņĀäļ¼╝ļĪ£ņä£ ņäØņČ£ļÉśņ¢┤ ļ¦ēņØä ņśżņŚ╝ņŗ£Ēé¼ ņłś ņ׳ļŗż. ļśÉ ĒĢśļéśļŖö ļ¦ēņØä ĒåĄĒĢ£ ļ¼╝ņØś ņØ┤ļÅÖĒśäņāüņ£╝ļĪ£, ĒؼņäØņŗżņŚÉņä£ ļåŹņČĢņŗżļĪ£ ļ¼╝ņØ┤ ņØ┤ļÅÖĒĢśņŚ¼ ļåŹņČĢņ£©ņØä Ļ░Éņåīņŗ£ĒéżļŖö ĒśäņāüņØ┤ļŗż.
ļ¼╝ņØ┤ ņØ┤ļÅÖĒĢśļŖö ņŻ╝ņÜö ņøÉņØĖņ£╝ļĪ£ ņØ┤ņś© ļåŹļÅäņ░©ņŚÉ ņØśĒĢ£ ņé╝Ēł¼ņĢĢ ĒśäņāüĻ│╝ ņłśĒÖöļÉ£ ņØ┤ņś©ņØ┤ ņĀäņ£äĻĄ¼ļ░░ ĒĢśņŚÉ ņØ┤ļÅÖņŗ£ ļ¼╝ļÅä ĒĢ©Ļ╗ś ņØ┤ļÅÖļÉśļŖö ņĀäĒĢ┤ņé╝Ēł¼(electro-osmosis) ĒśäņāüņØ┤ ņ׳ļŗż [16,17]. ņØ┤ļ¤¼ĒĢ£ ļæÉ Ēśäņāü ļ¬©ļæÉ ņŚ░ĻĄ¼ ļ░Å ņé░ņŚģĒśäņןņŚÉņä£ ņŻ╝ņÜöĒĢ£ ļ│ĆņłśļĪ£ņŹ© Ļ│ĄņĀĢ ņĀä ĒĢ£Ļ│äņĀäļźśļ░ĆļÅäļź╝ ļ»Ėļ”¼ ĒÖĢņØĖĒĢ┤ļæÉņ¢┤ņĢ╝ ĒĢśĻ│Ā, Ļ│ĄņĀĢ ņżæ ļ¼╝ ņØ┤ļÅÖĒśäņāüņØä ņĄ£ņåīĒÖö ĒĢśļŖö Ļ▓āņØä Ļ│ĀļĀżĒĢśņŚ¼ņĢ╝ ĒĢ£ļŗż.
ņØ╝ļ░śņĀüņ£╝ļĪ£ ņĀäĻĖ░Ēł¼ņäØņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņŚ╝ņØä ļåŹņČĢņŗ£ĒéżļŖö ļ░®ļ▓Ģņ£╝ļĪ£ļŖö High Volume Ratio Concentration(HVRC)ņÖĆ Multistage Concentration(MSC)ņØä ĒåĄĒĢ┤ ņØ┤ļŻ©ņ¢┤ņ¦äļŗż. HVRC ļ░®ņŗØņØĆ ļåŹņČĢņŗżĻ│╝ ĒؼņäØņŗżņØś ļČĆĒö╝ļ╣äļź╝ ņĪ░ņĀłĒĢśņŚ¼ ņøÉĒĢśļŖö ņä▒ļČäņØä ļåŹņČĢĒĢśļŖö ļ░®ņŗØņ£╝ļĪ£, ĒؼņäØņŗżņŚÉņä£ ļåŹņČĢņŗżļĪ£ ņŚ╝ņØ┤ ņŚ░ņåŹņĀüņ£╝ļĪ£ ņØ┤ļÅÖĒĢśņŚ¼ ļåŹņČĢĒĢśĻ▓ī ļÉ£ļŗż. MSC ļ░®ņŗØņØĆ 2ļŗ© ņØ┤ņāüņØś ņĀäĻĖ░Ēł¼ņäØņØä ĒåĄĒĢ┤ Ļ│ĀļåŹļÅäņØś ļåŹņČĢņÜ®ņĢĪņØä ņ¢╗ļŖö Ļ│ĄņĀĢņØ┤ļŗż. ņØ╝ļ░śņĀüņ£╝ļĪ£ HVRC ļ░®ņŗØņŚÉņä£ ļåŹņČĢņŚÉ ņĀüĒĢ®ĒĢ£ ņĄ£ņĀüņĪ░Ļ▒┤ņØä ĒÖĢļ”ĮĒĢ£ Ēøä MSC ļ░®ņŗØņ£╝ļĪ£ Ļ│ĀļåŹļÅäņØś ņÜ®ņĢĪņØä ņ¢╗Ļ▓ī ļÉ£ļŗż [17]. ļö░ļØ╝ņä£ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö 1ņ░©ņĀüņ£╝ļĪ£ HVRC ļ░®ņŗØņØä ņØ┤ņÜ®ĒĢśņŚ¼ ļ”¼ĒŖ¼ĒĢ©ņ£Ā ņøÉļŻīņÜ®ņĢĪņ£╝ļĪ£ļČĆĒä░ ļ”¼ĒŖ¼ņØä ļåŹņČĢĒĢśĻ│Āņ×É ĒĢśņśĆĻ│Ā, ļåŹņČĢņŗż ļé┤ ļ”¼ĒŖ¼ņØś ļåŹļÅä, ļ¼╝ ĒÜīņłśņ£©(ņØ┤ļÅÖņ£©), ĒÅēĻĘĀ ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ē, ĒÅēĻĘĀ ņ£Āļ¤ēņØś ņØĖņ×ÉļōżņØä Ļ│ĀļĀżĒĢśņŚ¼ ņĄ£ņĀü ņĪ░Ļ▒┤ņØä ļÅäņČ£ĒĢśĻ│Āņ×É ĒĢśņśĆļŗż.
3. ņŗżĒŚś ņןņ╣ś ļ░Å ļ░®ļ▓Ģ3.1 ņŗżĒŚś ņןņ╣śņĀäĻĖ░Ēł¼ņäØĻ│ĄņĀĢņŚÉ ņØśĒĢśņŚ¼ ļ”¼ĒŖ¼ņØä ļåŹņČĢņŗ£ĒéżĻĖ░ ņ£äĒĢ£ ņןņ╣śļĪ£ CJT-055 Electro Dialyzer(Chang Jo Tech. Co., Korea)ņØä ņé¼ņÜ®ĒĢśņśĆņ£╝ļ®░ ņןņ╣śņØś ņé¼ņ¦ä ļ░Å ņŻ╝ņÜöņé¼ņ¢æņØä ĻĘĖļ”╝ 2Ļ│╝ Ēæ£ 1ņŚÉ ļéśĒāĆļé┤ņŚłļŗż. ļåŹņČĢņŗż(concentrate tank), ĒؼņäØņŗż(dilute tank), ņĀäĻĘ╣ņŗż(electrode tank), ņĀĢļźśĻĖ░ ļō▒ņ£╝ļĪ£ ņ╣┤ĒŖĖļ”¼ņ¦ĆļŖö 10ņīŹņØś NEOSEPTA CSE┬ĘASE(ASTOM Co., Japan)ņŚÉ ņČöĻ░ĆļĪ£ 1ņןņØś CSEļĪ£ ņØ┤ļŻ©ņ¢┤ņĀĖņ׳Ļ│Ā Ļ░ü ĻĄÉĒÖśļ¦ē ņé¼ņØ┤ņŚÉ ļ╣ä ņĀłņŚ░ļ¼╝ņØś ņŖżĒÄśņØ┤ņä£Ļ░Ć ņ£äņ╣śĒĢśņŚ¼ Ļ░ĆņŖżņ╝ō ļ░Å ņĢĪņŗżņØä ĒśĢņä▒ĒĢśĻ│Ā ņ׳ļŗż. ņØ┤ņś©ĻĄÉĒÖśļ¦ēņØś ĒŖ╣ņä▒ņØĆ Ēæ£ 2ņŚÉ ļéśĒāĆļé┤ņŚłļŗż. ņĀĢļźśĻĖ░ļŖö DC, ņĀäņĢĢ 0~30 V, ņĀäļźś 0~5 AņØś ļ▓öņ£ä ļé┤ņŚÉņä£ ņ×æļÅÖĒĢśļéś ņ╣┤ĒŖĖļ”¼ņ¦Ć ļ░Å ņןņ╣śļ│┤ĒśĖļź╝ ņ£äĒĢ£ ņĀäļźśņØś ņāüĒĢ£ņäĀņØĆ 3 AņØ┤ļ®░ ņ¢æĻĘ╣ ļ░Å ņØīĻĘ╣ņ£╝ļĪ£ļŖö ļ░▒ĻĖłņØ┤ ņĮöĒīģļÉ£ Ēŗ░ĒāĆļŖäņØä ņé¼ņÜ®ĒĢśņśĆļŗż.
3.2 ņŗżĒŚś ļ░®ļ▓Ģļ”¼ĒŖ¼ ĒĢ©ņ£Ā ņøÉļŻīņÜ®ņĢĪ ļé┤ ļ”¼ĒŖ¼ņØś ļåŹņČĢņØä ņ£äĒĢśņŚ¼ ļåŹņČĢņŗżĻ│╝ ĒؼņäØņŗżņŚÉ ļ”¼ĒŖ¼ĒĢ©ņ£Ā ņøÉļŻīņÜ®ņĢĪņØä ņé¼ņÜ®ĒĢśņśĆĻ│Ā ņĀäĻĘ╣ņŗżņŚÉļŖö 0.3 M Na2SO4ļź╝ ņé¼ņÜ®ĒĢśņśĆņ£╝ļ®░ Ēæ£ 3ņŚÉ ņøÉļŻīņÜ®ņĢĪ ļé┤ ņĪ░ņä▒ņØä ļéśĒāĆļé┤ņŚłņ£╝ļ®░ ļČłņł£ļ¼╝ ņżæ P, Mg, Ca ļåŹļÅäļŖö 0.005 g/L ļ»Ėļ¦īņ£╝ļĪ£ Li, Na ļīĆļ╣ä ļ¦żņÜ░ ļé«ņĢśļŗż. ļśÉĒĢ£ ĒÄīĒöä ņ×æļÅÖ Ēøä ņ╣┤ĒŖĖļ”¼ņ¦Ć ļśÉļŖö ĒŖ£ļĖī ļé┤ ņĪ┤ņ×¼ĒĢśļŖö Ļ│ĄĻĖ░ļź╝ ņĀ£Ļ▒░ĒĢśĻĖ░ ņ£äĒĢ┤ 5ļČä ļÅÖņĢł ņÜ®ņĢĪņØä ņČ®ļČäĒ׳ ņł£ĒÖśņŗ£Ēé© Ēøä ņĀäņĢĢņØä ņØĖĻ░ĆĒĢśņśĆļŗż. ņØ┤Ēøä 15ļČäļ¦łļŗż ļåŹņČĢņŗżĻ│╝ ĒؼņäØņŗżņØś ņĀäĻĖ░ņĀäļÅäļÅäļź╝ ņĖĪņĀĢĒĢśņśĆņ£╝ļ®░ ĒؼņäØņŗżņØś ņĀäĻĖ░ņĀäļÅäļÅäĻ░Ć 1.00 mS/cm ņØ┤ĒĢśĻ░Ć ļÉĀ ļĢī ņŗżĒŚśņØä ņóģļŻīĒĢśņśĆļŗż [17,18]. ņŚ¼ĻĖ░ņä£ S(siemens)ļŖö ņĀäļÅäļÅäņØś ļŗ©ņ£äļĪ£ ņĀäĻĖ░ņĀĆĒĢŁņØś ļŗ©ņ£ä ņś┤(╬®)ņØś ņŚŁņłśņØ┤ļ®░ 1 S = 1 A/V = 1/╬® ņØ┤ļŗż. ņŗżĒŚś ņóģļŻī Ēøä ļåŹņČĢņŗż, ĒؼņäØņŗż ļ░Å ņĀäĻĘ╣ņŗżņŚÉņä£ Ļ░üĻ░ü ņāśĒöīņØä ņ▒äņĘ©ĒĢśņŚ¼ ICP-AES (Perkin Elmer/Optima-4300 DV)ļĪ£ ļČäņäØĒĢśņśĆļŗż. ļåŹļÅäĻ░Ć ļé«ņØĆ P, Mg, CaļŖö ņĀäĻĖ░ Ēł¼ņäØ ņżæ ņØ┤ņś© ņØ┤ļÅÖņØ┤ ņØ╝ņ¢┤ļéśņ¦Ć ņĢŖņĢä ņŗżĒŚś Ļ▓░Ļ│╝ņŚÉņä£ļŖö Li, Na, SO4ņŚÉ ļīĆĒĢ£ Ļ▒░ļÅÖļ¦ī ļéśĒāĆļé┤ņŚłļŗż. ņĀäļźśņÖĆ ņĀäļźśļ░ĆļÅä ņé¼ņØ┤ņØś Ļ┤ĆĻ│äņŗØņØä ņŗØ (1)ņŚÉ ļéśĒāĆļé┤ņŚłĻ│Ā, ņØ┤ņś© ļåŹļÅä, ņŗżĒŚś Ēøä ņÜ®ņĢĪ ļČĆĒö╝, Ļ│ĄņĀĢņŚÉ ņåīņÜöļÉ£ ņŗ£Ļ░ä ļō▒ņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņŗØ(2) Ōł╝ (4)ņŚÉ ņØśĒĢ┤ Ļ░ü ņĪ░Ļ▒┤ņŚÉņä£ņØś ļ¼╝ ĒÜīņłśņ£©, ĒÅēĻĘĀ ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ē, ĒÅēĻĘĀņ£Āļ¤ēņØĆ Y. ZhouņŚÉ ņØśĒĢ┤ ņĀ£ņŗ£ļÉ£ ņŗØņØä ņØ┤ņÜ®ĒĢśņŚ¼ Ļ│äņé░ĒĢśņśĆļŗż [17]. ņĀäļźśļ░ĆļÅäņÖĆ ņĀäļźś ņé¼ņØ┤ņØś ļ│ĆĒÖś ņŗØņØä ņŗØ (4)ņŚÉ ļéśĒāĆļé┤ņŚłļŗż.
ņĀäĻĖ░Ēł¼ņäØ ņןņ╣śņŚÉņä£ ĻĖ░ļĪØļÉ£ ņĀäļźś Ļ░ÆņØä ņĀäļźśļ░ĆļÅä Ļ░Æņ£╝ļĪ£ ļ│ĆĒÖöĒĢśĻĖ░ ņ£äĒĢ┤ ļŗżņØīĻ│╝ Ļ░ÖņØĆ ņŗØņØä ņé¼ņÜ®ĒĢśņśĆņ£╝ļ®░, I(A)ļŖö ņĀäļźś, J(A/dm2)ļŖö ņĀäļźśļ░ĆļÅä, AļŖö ņØ┤ņś©ĻĄÉĒÖśļ¦ēņØś ņ£ĀĒÜ©ļ®┤ņĀü(dm2)ņØä ļéśĒāĆļéĖļŗż.
ļ¼╝ ĒÜīņłśņ£©(W, %)ņØĆ ļŗżņØīĻ│╝ Ļ░ÖņØĆ ņŗØņ£╝ļĪ£ ĻĄ¼ĒĢĀ ņłś ņ׳ņ£╝ļ®░ V0ņÖĆ VtļŖö Ļ░üĻ░ü 0ļČäĻ│╝ tļČä Ēøä ĒؼņäØņŗżņØś ļČĆĒö╝(L)ļź╝ ļéśĒāĆļéĖļŗż.
ĒÅēĻĘĀ ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ē(E, kWh/m3)ņØĆ ļŗżņØīĻ│╝ Ļ░ÖņØĆ ņŗØņ£╝ļĪ£ ĻĄ¼ĒĢĀ ņłś ņ׳ņ£╝ļ®░ U(V)ļŖö ņØĖĻ░ĆņĀäņĢĢ, I(A)ļŖö ņØĖĻ░ĆļÉ£ ņĀäļźś, V(L)ņØĆ ņ┤łĻĖ░ ļ”¼ĒŖ¼ņÜ®ņĢĪņØś ļČĆĒö╝ņØ┤ļŗż.
ĒÅēĻĘĀ ņ£Āļ¤ē(J, mol/m2h)ņØĆ ļŗżņØīĻ│╝ Ļ░ÖņØĆ ņŗØņ£╝ļĪ£ ĻĄ¼ĒĢĀ ņłś ņ׳ņ£╝ļ®░, mņØĆ ļåŹņČĢņŗżņŚÉņä£ ļåŹņČĢļÉ£ LiņØś ņ¦łļ¤ē(g), NņØĆ ĻĄÉļīĆļĪ£ ņ£äņ╣śĒĢ£ ņ¢æņØ┤ņś© ĻĄÉĒÖśļ¦ēĻ│╝ ņØīņØ┤ņś© ĻĄÉĒÖśļ¦ēņØś ņīŹ Ļ░£ņłś, AļŖö ņØ┤ņś©ĻĄÉĒÖśļ¦ēņØś ņ£ĀĒÜ©ļ®┤ņĀü(m2), MņØĆ ļåŹņČĢļÉ£ ļ”¼ĒŖ¼ņØś ļČäņ×Éļ¤ē(g/mol), tļŖö Ēł¼ņäØ ņŗ£Ļ░ä(hr)ņØä ļéśĒāĆļéĖļŗż.
4. ņŗżĒŚś Ļ▓░Ļ│╝ ļ░Å Ļ│Āņ░░4.1 ĒĢ£Ļ│äņĀäļźśļ░ĆļÅäņĀäĻĖ░Ēł¼ņäØ ņŗ£ ņÜ®ņĢĪņżæņØś ļåŹļÅäĻ░Ć ņŚ░ņåŹņĀüņ£╝ļĪ£ ļ│ĆĒĢśĻ▓ī ļÉśļŖöļŹ░ ļ░śņØæ ļÅäņżæņŚÉ ĒĢ£Ļ│äņĀäļźśļ░ĆļÅäļź╝ ņ┤łĻ│╝ĒĢĀ Ļ▓ĮņÜ░ ņĀäļĀźņØ┤ ĒĢäņÜöņØ┤ņāüņ£╝ļĪ£ ņåīļ╣äļÉśļŖö Ļ▓āņØä ļ░®ņ¦ĆĒĢśĻ│Ā, ļśÉĒĢ£ ņÜ®ņĢĪ ņżæ pHņØś ļ│ĆĒÖöņŚÉ ļö░ļØ╝ ļ¦ē Ēæ£ļ®┤ņŚÉ ņŖżņ╝ĆņØ╝ ĒśĢņä▒ņŚÉ ņØśĒĢ£ ļ¦ē ņåÉņāüņØä ļ░®ņ¦ĆĒĢśĻĖ░ ņ£äĒĢśņŚ¼ ņÜ®ņĢĪļåŹļÅäņŚÉ ļö░ļźĖ ĒĢ£Ļ│äņĀäļźśļ░ĆļÅäļź╝ ņĖĪņĀĢĒĢśņśĆļŗż [16]. ņŗżĒŚśņØĆ ņĀäņĢĢņØĖĻ░Ć Ēøä 1ļČä ļÅÖņĢł ņĢłņĀĢĒÖöĒĢ£ ļÆż ņĀäļźś ļ░ĆļÅä Ļ░ÆņØä ņĖĪņĀĢĒĢśņśĆņ£╝ļ®░ ņĀäļźś-ņĀäņĢĢ Ļ│ĪņäĀņŚÉņä£ ĻĖ░ņÜĖĻĖ░Ļ░Ć ļ│ĆĒĢśļŖö ņ¦ĆņĀÉņØä ĒåĄĒĢ┤ ĒĢ£Ļ│äņĀäļźśļź╝ ņĢīņĢäļ│┤ņĢśĻ│Ā ņØ┤ņŚÉ ļīĆĒĢ£ Ļ▓░Ļ│╝ļź╝ ĻĘĖļ”╝ 3ņŚÉ ļéśĒāĆļé┤ņŚłļŗż. ņŗżĒŚśņŚÉ ņé¼ņÜ®ļÉ£ ņÜ®ņĢĪņØĆ Ēæ£ 3ņØś ņĪ░ņä▒ņØä Ļ░Ćņ¦ĆļŖö ļ”¼ĒŖ¼ ĒĢ©ņ£Ā ņøÉļŻīņÜ®ņĢĪĻ│╝, Ēæ£ 4ņØś ņĪ░ņä▒ņØä Ļ░Ćņ¦ĆļŖö ļåŹļÅäņĪ░ņĀłņØä ņ£äĒĢ£ ļ¬©ņØśņÜ®ņĢĪņØä ņĀ£ņĪ░ĒĢśņŚ¼ ņé¼ņÜ®ĒĢśņśĆļŗż. ņØ╝ļ░śņĀüņ£╝ļĪ£ ĒĢ£Ļ│äņĀäļźśļ░ĆļÅä(ilim)ņÖĆ ņØ┤ņś© ļåŹļÅä(Cb) ņé¼ņØ┤ņØś Ļ┤ĆĻ│äņŗØņØĆ ņŗØ (5)ņÖĆ Ļ░ÖņØ┤ ĒÖĢņé░Ļ│äņłś(D), Faraday ņāüņłś(F), ņØ┤ņś©ĻĄÉĒÖś ļ¦ē ļé┤ ņØ┤ļÅÖņłś(tm), ņÜ®ņĢĪ ļé┤ ņØ┤ļÅÖņłś(ts), ĒÖĢņé░ņĖĄ ļæÉĻ╗ś(╬┤)ņŚÉ ņØśĒĢ┤ ņĀĢņØś ļÉĀ ņłś ņ׳ņ£╝ļ®░ [19,20], ņØ┤ņś© ļåŹļÅäņÖĆ ĒĢ£Ļ│äņĀäļźś Ļ░ÆņØĆ ļ╣äļĪĆ Ļ┤ĆĻ│äņØ┤ļŗż. ņĀäĻĖ░Ēł¼ņäØņØ┤ ņ¦äĒ¢ēļÉśļŖö ļÅÖņĢł ĒāłņŚ╝ļÉśņ¢┤ ņÜ®ņĢĪ ņżæ ņØ┤ņś© ļåŹļÅäĻ░Ć Ļ░ÉņåīĒĢ©ņŚÉ ļö░ļØ╝ ĒĢ£Ļ│äņĀäļźśĻ░Ć ļéśĒāĆļéĀ ņłś ņ׳ņ¢┤ [21], ļ¬©ņØś ņÜ®ņĢĪ ņżæ ļ”¼ĒŖ¼ ņØ┤ņś© ļåŹļÅäļź╝ 5.0 g/LņŚÉņä£ 0.1 g/L ņłśņżĆĻ╣īņ¦Ć ĒؼņäØĒĢśņŚ¼ ņØĖĻ░ĆņĀäņĢĢņŚÉ ļö░ļźĖ ņĀäļźś ļ░ĆļÅäļź╝ Ļ│Āņ░░ĒĢśņśĆļŗż. ĻĘĖļ”╝ 3ņ£╝ļĪ£ļČĆĒä░ ņØĖĻ░ĆņĀäņĢĢ 16 V ņØ┤ĒĢśņŚÉņä£ļŖö ņØĖĻ░ĆņĀäņĢĢņŚÉ ļö░ļØ╝ ņĀäļźśļ░ĆļÅäĻ░Ć ļ╣äļĪĆĒĢ┤ņä£ ņ”ØĻ░ĆĒĢśļŖö Ļ▓ĮĒ¢źņØä ļ│┤ņśĆĻ│Ā, ļśÉĒĢ£ ļÅÖņØ╝ĒĢ£ ņØĖĻ░ĆņĀäņĢĢņŚÉņä£ ņØ┤ņś© ļåŹļÅäĻ░Ć Ļ░ÉņåīĒĢ©ņŚÉ ļö░ļØ╝ ņĀäļźśļ░ĆļÅäļÅä Ļ░ÉņåīĒĢśļŖö Ļ▓ĮĒ¢źņØä ļéśĒāĆļé┤ĻĖ░ ļĢīļ¼ĖņŚÉ ĒĢ£Ļ│äņĀäļźśļ░ĆļÅäļŖö Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśļŗż. ļśÉĒĢ£, ņŗżĒŚś ņóģļŻī ņĀä Ēøä ļåŹņČĢņŗżĻ│╝ ĒؼņäØņŗżņØś pHļź╝ ĒÖĢņØĖĒĢ£ Ļ▓░Ļ│╝ pH 6~7 ņé¼ņØ┤ļĪ£ Ēü░ ļ│ĆĒÖöļŖö ņŚåņŚłļŗż.
4.2 ņØĖĻ░ĆņĀäņĢĢ ņśüĒ¢ź Ļ│Āņ░░ņĀĢņĀäņĢĢ ņĪ░Ļ▒┤ņŚÉņä£ ņĀäņĢĢņŚÉ ļö░ļźĖ ļ”¼ĒŖ¼ ļåŹņČĢņØś ņĀüņĀĢņĪ░Ļ▒┤ņØä Ļ│Āņ░░ĒĢśĻĖ░ ņ£äĒĢśņŚ¼ ĒؼņäØņŗż, ļåŹņČĢņŗż, ņĀäĻĘ╣ņŗżņŚÉ ņÜ®ņĢĪņØä Ļ░üĻ░ü 400 mLņö® ņé¼ņÜ®ĒĢśņŚ¼ ņŗżĒŚśņØä ņ¦äĒ¢ēĒĢśņśĆļŗż. ņĀäĻĖ░Ēł¼ņäØ ņżæ ņŗ£Ļ░äņŚÉ ļö░ļźĖ ņĀäĻĖ░ņĀäļÅäļÅäļź╝ ĻĘĖļ”╝ 4ņŚÉ ļéśĒāĆļé┤ņŚłņ£╝ļ®░ ņØ┤ ļĢī DļŖö ĒؼņäØņŗż, CļŖö ļåŹņČĢņŗżņØä ļ£╗ĒĢ£ļŗż. Ēæ£ 5ņŚÉļŖö ņŗżĒŚś Ēøä ļåŹņČĢņŗżņŚÉņä£ņØś Li+, Na+, SO42- ņØ┤ņś©ņØś ļåŹļÅäļź╝ ļéśĒāĆļé┤ņŚłļŖöļŹ░ ņØĖĻ░ĆņĀäņĢĢņØ┤ ļåÆņØäņłśļĪØ ļåŹņČĢļÉ£ ļ”¼ĒŖ¼ņØś ļåŹļÅäĻ░Ć ļåÆņØīņØä ļ│┤ņśĆļŗż. ņØ┤Ēøä ņŗØ (2)~(4)ņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ēĻ│╝ ĒÅēĻĘĀņ£Āļ¤ēņØä Ļ│äņé░ĒĢ£ Ļ▓░Ļ│╝ļź╝ Ēæ£ 6ņŚÉ ļéśĒāĆļé┤ņŚłņ£╝ļ®░ ņĀäņĢĢņØ┤ ļåÆņØäņłśļĪØ ņĀäļĀź ņåīļ╣äļ¤ēņØ┤ ļ¦ÄĻĖ░ ļĢīļ¼ĖņŚÉ ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ēņØ┤ ļåÆņĢśņ£╝ļ®░ ļśÉĒĢ£ Ļ│ĄņĀĢņŚÉ ņåīņÜöļÉśļŖö ņŗ£Ļ░äņØ┤ ņ¦¦ņĢä ĒÅēĻĘĀņ£Āļ¤ēņØ┤ ļåÆņĢśļŗż. ņŚ¼ļ¤¼ ņØĖņ×ÉļōżņØä Ļ│ĀļĀżĒĢśņśĆņØä ļĢī 12 VņŚÉņä£ Ļ░Ćņן ļ╣Āļź┤Ļ▓ī ļ”¼ĒŖ¼ņØä ļåŹņČĢņŗ£Ēé¼ ņłś ņ׳Ļ│Ā ļ¼╝ ĒÜīņłśņ£©, ļ”¼ĒŖ¼ ņŗżĒŚś Ēøä ļåŹļÅä ļ░Å ĒÅēĻĘĀ ņ£Āļ¤ēņØ┤ Ļ░Ćņן ļåÆņĢśņ£╝ļéś ņØīĻĘ╣ņŚÉņä£ ĒÖśņøÉļÉśļŖö ņłśņåīĻĖ░ņ▓┤ņŚÉ ņØśĒĢ┤ ņØīĻĘ╣Ļ│╝ ņĀäĻĘ╣ņŗż ņé¼ņØ┤ņŚÉ ļåŹļÅäļČäĻĘ╣ņØ┤ Ēü¼Ļ▓ī ņØ╝ņ¢┤ļéśĻ▓ī ļÉśĻ│Ā ņĀäĻĘ╣ņŗż ņåŹ ņØ┤ņś©ņØ┤ ņØīĻĘ╣ņŚÉ ĒÖśņøÉļÉśļŖö ĒśäņāüņØ┤ ļéśĒāĆļéś ņןņ╣śņŚÉ ļ¼ĖņĀ£ļź╝ ņØ╝ņ£╝Ēé¼ ņłś ņ׳ņ¢┤ ņĀüņĀłĒĢśņ¦Ć ņĢŖļŗż. 12 Vļź╝ ņĀ£ņÖĖĒĢśĻ│Ā ņĀäĻĖ░Ēł¼ņäØņŚÉ ņåīņÜöļÉśļŖö ņŗ£Ļ░ä, ļ¼╝ ĒÜīņłśņ£©, ĒÅēĻĘĀ ņ£Āļ¤ēņØś ņØĖņ×ÉļōżņØä Ļ│ĀļĀżĒĢśņśĆņØä ļĢī 10 VĻ░Ć ņĀüņĀĢņĪ░Ļ▒┤ņØ┤ļ®░ ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ē ņĖĪļ®┤ņŚÉņä£ļŖö 8 VĻ░Ć ņĀüņĀĢņĪ░Ļ▒┤ņØ┤ļŗż. ņØ┤ ļĢī ņĀäĻĖ░Ēł¼ņäØ ņŗ£ ļ¼╝ņØ┤ ņØ┤ļÅÖļÉśļŖö ĒśäņāüņŚÉ ņØśĒĢ┤ ņŗżĒŚś Ēøä ļåŹļÅäĻ░Ć Ļ░ÉņåīĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ĒؼņäØņŗżĻ│╝ ļåŹņČĢņŗżņØś ļČĆĒö╝ļ╣äļź╝ ņĪ░ņĀłĒĢśļŖö ņČöĻ░ĆņĀüņØĖ ņĪ░ņ×æņØ┤ ņÜöĻĄ¼ļÉ£ļŗż.
4.3 ļČĆĒö╝ļ╣ä ļ│ĆĒÖö ņśüĒ¢ź Ļ│Āņ░░ĒؼņäØņŗżĻ│╝ ļåŹņČĢņŗżņØś ļČĆĒö╝ļ╣ä ņĪ░ņĀłņŚÉ ņØśĒĢ£ ļ”¼ĒŖ¼ļåŹņČĢņØś ņĀüņĀĢņĪ░Ļ▒┤ņØä Ļ│Āņ░░ĒĢśņśĆļŗż. ļåŹņČĢņŗżĻ│╝ ņĀäĻĘ╣ņŗżņØś ņÜ®ņĢĪņØĆ Ļ░üĻ░ü 400 mLņö® ņé¼ņÜ®ĒĢśņśĆĻ│Ā, ļČĆĒö╝ļ╣ä ņĪ░ņĀłņØä ņ£äĒĢ┤ ĒؼņäØņŗżņØĆ 400, 800, 1200, 1600 mL ņö® ņé¼ņÜ®ĒĢśņśĆļŗż. 8 VņÖĆ 10 VņØś ņĀĢņĀäņĢĢ ņĪ░Ļ▒┤ņŚÉņä£ ņŗżĒŚśņØä ņ¦äĒ¢ēĒĢśņśĆĻ│Ā ĻĘĖļ”╝ 5(a)ņŚÉļŖö 8 VņØ╝ ļĢī, ĻĘĖļ”╝ 5(b)ņŚÉļŖö 10 VņØ╝ ļĢī ņŗ£Ļ░äņŚÉ ļö░ļźĖ ņĀäĻĖ░ņĀäļÅäļÅäļź╝ ļéśĒāĆļé┤ņŚłņ£╝ļ®░ ĻĘĖļ”╝ 6Ļ│╝ Ēæ£ 7ņŚÉļŖö ņŗżĒŚś Ēøä ļåŹņČĢņŗżņŚÉņä£ Li+, Na+, SO42- ņØ┤ņś©ņØś ļåŹļÅäļź╝ ļéśĒāĆļé┤ņŚłĻ│Ā ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ē, ĒÅēĻĘĀ ņ£Āļ¤ēņØä Ļ│äņé░ĒĢśņŚ¼ ĻĘĖļ”╝ 7(a), (b)ņŚÉ ļéśĒāĆļé┤ņŚłļŗż. ņØ┤ ļĢī VDļŖö ĒؼņäØņŗżņØś ļČĆĒö╝, VCļŖö ļåŹņČĢņŗżņØś ļČĆĒö╝ļź╝ ļ£╗ĒĢ£ļŗż.
ļ¼╝ ĒÜīņłśņ£©ņØĆ 8 VņØ╝ ļĢī ĒÅēĻĘĀ 25.07 %, 10 V ņØ╝ ļĢī ĒÅēĻĘĀ 30.85 %ļĪ£ ņĀäņĢĢņØ┤ ļåÆņØä ļĢī ņĀäĻĖ░Ēł¼ņäØ Ļ│ĄņĀĢņŚÉ ņåīņÜöļÉśļŖö ņŗ£Ļ░äņØ┤ Ļ░ÉņåīĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ļŹö ļåÆņØĆ ļ¼╝ ĒÜīņłśņ£©ņØä ļ│┤ņśĆļŗż. ĻĘĖļ”╝ 6ņŚÉņä£ ļ”¼ĒŖ¼ ņŗżĒŚś Ēøä ļåŹļÅäļŖö 8, 10 VņØś ņĀĢņĀäņĢĢ ņĪ░Ļ▒┤ņŚÉņä£ ļ¬©ļæÉ ļČĆĒö╝ļ╣ä(VD/VC)ņŚÉ ļ╣äļĪĆĒĢśņŚ¼ ņ”ØĻ░ĆĒĢśņśĆĻ│Ā 10 V ņØ╝ ļĢī ļ”¼ĒŖ¼ņØś ņŗżĒŚś Ēøä ļåŹļÅäĻ░Ć ļŹö Ēü░ ĒÅŁņ£╝ļĪ£ ņ”ØĻ░ĆĒĢśņśĆļŗż. ĻĘĖļ”╝ 7(a)ņØś ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ēņØĆ ļ¬©ļōĀ ļČĆĒö╝ļ╣ä ņĪ░Ļ▒┤ņŚÉņä£ 10 V ņØ╝ ļĢī ļŹö ļåÆņØĆ Ļ░ÆņØä ļ│┤ņśĆĻ│Ā, ļČĆĒö╝ļ╣äņŚÉ ļ╣äļĪĆĒĢśņŚ¼ ņ”ØĻ░ĆĒĢśņśĆļŖöļŹ░ ņØ┤Ļ▓āņØĆ Ļ│ĄņĀĢņŚÉ ņåīņÜöļÉśļŖö ņŗ£Ļ░äņØ┤ ĻĖĖņ¢┤ņĪīĻĖ░ ļĢīļ¼ĖņØ┤ļØ╝ ņé¼ļŻīļÉ£ļŗż. ļśÉĒĢ£ ĻĘĖļ”╝ 7(b)ņØś ĒÅēĻĘĀ ņ£Āļ¤ē ļśÉĒĢ£ 10 V ņØ╝ ļĢī ļåÆņĢśņ£╝ļ®░ ļČĆĒö╝ļ╣äņŚÉ ļ╣äļĪĆĒĢśņŚ¼ Ļ░ÉņåīĒĢśņśĆĻ│Ā ļČĆĒö╝ļ╣äĻ░Ć ņ╗żņ¦łņłśļĪØ ļ¦ē ļ®┤ņĀüļŗ╣ ĒؼņäØņŗżņŚÉņä£ ļåŹņČĢņŗżļĪ£ ņØ┤ļÅÖĒĢśļŖö ņØ┤ņś©ņØś ņ¢æņØ┤ ļŹö ļ¦ÄņĢäņ¦ĆĻĖ░ ļĢīļ¼ĖņØ┤ļØ╝ ņé¼ļŻīļÉ£ļŗż. ĒĢ£ĒÄĖ CJMA/MAļź╝ ņØ┤ņś©ĻĄÉĒÖśļ¦ēņ£╝ļĪ£ ņé¼ņÜ®ĒĢ£ ļ”¼ĒŖ¼ ļåŹņČĢ ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļČĆĒö╝ļ╣äĻ░Ć ņ”ØĻ░ĆĒĢĀņłśļĪØ ņŗżĒŚś Ēøä ļåŹļÅä ļśÉĒĢ£ ņ”ØĻ░ĆĒĢ©ņØä ļ│┤ņśĆņ£╝ļéś, NEOSEPTA CMX┬ĘAMXļź╝ ņé¼ņÜ®ĒĢ£ ĒÖ®ņé░ļ”¼ĒŖ¼ ļåŹņČĢ ņŚ░ĻĄ¼ņŚÉņä£ļŖö ļČĆĒö╝ļ╣äņŚÉ ļ╣äļĪĆĒĢśņŚ¼ ļåŹņČĢļÉ£ ĒÖ®ņé░ļ”¼ĒŖ¼ņØś ļåŹļÅäĻ░Ć ņ”ØĻ░ĆĒĢśļŗż ĒĢ£Ļ│äņŚÉ ļÅäļŗ¼ĒĢśļĀżļŖö ĒśäņāüņØä ļ│┤ņØ┤Ļ│Ā ņ׳ņ¢┤ ļČĆĒö╝ļ╣äļź╝ ļŹö ņ”ØĻ░Ćņŗ£ņ╝£ ļåŹņČĢ Ļ▓ĮĒ¢źņØä Ļ│Āņ░░ĒĢĀ ĒĢäņÜöĻ░Ć ņ׳ļŗż [17,22].
High volume ratio concentration(HVRC) ļ░®ņŗØņØä ĒåĄĒĢ┤ ļ”¼ĒŖ¼ņØä ļåŹņČĢĒĢśĻĖ░ ņ£äĒĢśņŚ¼ ĒؼņäØņŗżĻ│╝ ļåŹņČĢņŗżņØś ļČĆĒö╝ļ╣ä(VD/VC)ļź╝ 1/1(900 mL / 900 mL) ~ 10/1(1,636 mL / 164 mL)Ļ╣īņ¦Ć ņĪ░ņĀłĒĢśņŚ¼ ņĀäĻĖ░Ēł¼ņäØ ņŗżĒŚśņØä ņŗżņŗ£ĒĢśņśĆļŗż. ņØ┤ļĢī ņØĖĻ░ĆņĀäņĢĢņØĆ 10 V ņØ┤ņŚłņ£╝ļ®░ ņĀäĻĘ╣ņŗżņŚÉļŖö 0.3 M Na2SO4ņÜ®ņĢĪņØä 500 mL ņé¼ņÜ®ĒĢśņśĆļŗż. ĻĘĖļ”╝ 8ņŚÉ ņŗ£Ļ░äņŚÉ ļö░ļźĖ ņĀäĻĖ░ņĀäļÅäļÅäļź╝ ļéśĒāĆļé┤ņŚłĻ│Ā, ĻĘĖļ”╝ 9ņÖĆ Ēæ£ 8ņŚÉļŖö ņŗżĒŚś Ēøä ļåŹņČĢņŗżņŚÉņä£ Li+, Na+, SO42- ņØ┤ņś©ņØś ļåŹļÅäļź╝ ļéśĒāĆļé┤ņŚłļŗż. ļśÉĒĢ£ ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ē, ĒÅēĻĘĀņ£Āļ¤ēņØä Ļ│äņé░ĒĢśņŚ¼ ĻĘĖļ”╝ 10(a), (b)ņŚÉ ļéśĒāĆļé┤ņŚłļŗż. ņØ┤ Ļ▓ĮņÜ░ ļ¼╝ĒÜīņłśņ£©ņØĆ ĒÅēĻĘĀ 37.24%ļĪ£ ņØ╝ņĀĢĒĢśņśĆĻ│Ā, ļ”¼ĒŖ¼ņØś ņŗżĒŚś Ēøä ļåŹļÅäļŖö ļČĆĒö╝ļ╣äņŚÉ ļ╣äļĪĆĒĢśņŚ¼ ņ”ØĻ░ĆĒĢśļŗżĻ░Ć Ļ░ÉņåīĒĢśļŖö Ļ▓ĮĒ¢źņØä ļ│┤ņśĆļŗż. HVRCĻ░Ć 9/1(1,620 mL / 180 mL)Ļ│╝ 10/1(1,636 mL /164 mL)ņØ╝ ļĢī ņŗżĒŚś Ēøä ļåŹļÅäĻ░Ć Ļ░ÉņåīĒĢśļŖö ņØ┤ņ£ĀļŖö ņÜ®ļ¦żņØĖ ļ¼╝Ēł¼Ļ│╝ņåŹļÅäĻ░Ć ņŚ╝ Ēł¼Ļ│╝ņåŹļÅäļ│┤ļŗż ļ╣Āļź┤ĻĖ░ ļĢīļ¼ĖņØ┤ļŗż. ņ”ē ņŗżĒŚś ĒøäĻĖ░ņŚÉ ļ¼╝ņØ┤ ņé╝Ēł¼ņĢĢ ĒśäņāüņŚÉ ņØśĒĢ┤ Ēł¼Ļ│╝ļÉśļŖö Ļ▓āņØ┤ ņ¦Ćļ░░ļ░śņØæņØ┤ ļÉ£ļŗż [17]. ĻĘĖļ”╝ 10(a)ņØś ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ēņØĆ ļČĆĒö╝ļ╣äņŚÉ ļ╣äļĪĆĒĢśņŚ¼ ņ”ØĻ░ĆĒĢśņśĆĻ│Ā ĻĘĖļ”╝ 10(b)ņØś ĒÅēĻĘĀ ņ£Āļ¤ēņØĆ Ļ░ÉņåīĒĢśņśĆļŗż. ļö░ļØ╝ņä£ ņāüĻĖ░ ņŗżĒŚśĻ▓░Ļ│╝ļĪ£ļČĆĒä░ ļ”¼ĒŖ¼ļåŹņČĢņ£©, ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ē, ĒÅēĻĘĀņ£Āļ¤ēņØä Ļ│ĀļĀżĒĢĀ Ļ▓ĮņÜ░ ļČĆĒö╝ļ╣ä 3/1(1,350 mL / 450 mL)ņØĖ ņĪ░Ļ▒┤ņØ┤ ļ”¼ĒŖ¼ ļåŹņČĢņŚÉ ņĀüņĀĢĒĢ£ ņĪ░Ļ▒┤ņØ┤ļØ╝Ļ│Ā ņāØĻ░üļÉ£ļŗż.
5. Ļ▓░ ļĪĀĒÅÉ ļ”¼ĒŖ¼ņØ┤ņś©ļ░░Ēä░ļ”¼ņŚÉņä£ ņ£ĀĻ░ĆĻĖłņåŹņØä ĒÜīņłśĒĢśĻ│Ā ļé©ņØĆ ņČöņČ£ņŚ¼ņĢĪņØä ņøÉļŻīņÜ®ņĢĪņ£╝ļĪ£ ĒĢśņŚ¼ ļ”¼ĒŖ¼ņØä ļČäļ”¼┬ĘļåŹņČĢĒĢśĻĖ░ ņ£äĒĢ┤ ņĀäĻĖ░Ēł¼ņäØņØä ņĀüņÜ®ĒĢśņŚ¼ ĻĖ░ņ┤łņŚ░ĻĄ¼ļź╝ ņŗżņŗ£ĒĢ£ Ļ▓░Ļ│╝, ļŗżņØīĻ│╝ Ļ░ÖņØĆ Ļ▓░ļĪĀņØä ņ¢╗ņØä ņłś ņ׳ņŚłļŗż.
1) Ļ│ĄņĀĢ ņĢłņĀĢņä▒ņØä ņ£äĒĢ┤ ĒĢ£Ļ│äņĀäļźśļ░ĆļÅäļź╝ ņĢīņĢäļ│Ė Ļ▓░Ļ│╝ ņÜ®ņĢĪ ļé┤ ņØ┤ņś© ļåŹļÅäĻ░Ć Ļ░ÉņåīĒĢĀņłśļĪØ ņĀäļźś ļ░ĆļÅä ļśÉĒĢ£ Ļ░ÉņåīĒĢśļŖö Ļ▓ĮĒ¢źņØä ļ│┤ņśĆņ£╝ļéś, ņøÉļŻī ņÜ®ņĢĪ ļåŹļÅäņØś 3% ņłśņżĆņŚÉņä£ļÅä ĒĢ£Ļ│äņĀäļźśļ░ĆļÅäĻ░Ć Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśļŗż.
2) ņØĖĻ░ĆņĀäņĢĢņŚÉ ļö░ļźĖ ņĀäĻĖ░Ēł¼ņäØ Ļ▓░Ļ│╝ Ļ│ĄņĀĢ ņåīņÜö ņŗ£Ļ░ä, ļ¼╝ĒÜīņłśņ£©, ĒÅēĻĘĀ ņ£Āļ¤ē, ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ēņØä Ļ│ĄņĀĢ ņØĖņ×ÉļĪ£ Ļ│ĀļĀżĒĢśņśĆņØä ļĢī ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ē Ļ┤ĆņĀÉņŚÉņä£ļŖö 8 VĻ░Ć ĒÜ©ņ£©ņĀüņØ┤ļéś, 10 V ņĪ░Ļ▒┤ņŚÉņä£ Ļ│ĄņĀĢ ņåīņÜö ņŗ£Ļ░äņØ┤ ņ¦¦Ļ│Ā ļ¼╝ ĒÜīņłśņ£©Ļ│╝ ĒÅēĻĘĀņ£Āļ¤ēņØ┤ ļåÆĻĖ░ ļĢīļ¼ĖņŚÉ Ļ│ĄņĀĢ ņÜ┤ņĀä ņĀäņĢĢņØĆ 10 VĻ░Ć ĒÜ©ņ£©ņĀüņØ┤ļŗż.
3) ĒؼņäØņŗżņØś ļČĆĒö╝ļź╝ ņ”ØĻ░Ćņŗ£ņ╝£ ĒؼņäØņŗżĻ│╝ ļåŹņČĢņŗżņØś ļČĆĒö╝ļ╣ä(VD/VC) ņĪ░ņĀłĒĢśņśĆņØä Ļ▓ĮņÜ░, ļČĆĒö╝ļ╣äĻ░Ć ņ”ØĻ░ĆĒĢśņŚ¼ļÅä ļ¼╝ Ēł¼Ļ│╝ņåŹļÅäļ│┤ļŗż ļ”¼ĒŖ¼ņØś Ēł¼Ļ│╝ ņåŹļÅäĻ░Ć ļŹö ļ╣©ļØ╝ ļ”¼ĒŖ¼ņØś ļåŹņČĢņ£©ņØ┤ ņ”ØĻ░ĆĒĢśņśĆņ£╝ļ®░, ņØĖĻ░ĆņĀäņĢĢ 10 V, ļČĆĒö╝ļ╣äĻ░Ć 4/1ņØ╝ ļĢī 4.4 g/LĻ╣īņ¦Ć ļåŹņČĢļÉśņŚłļŗż.
4) High volume ratio concentration (HVRC) ļ░®ņŗØņØä ņé¼ņÜ®ĒĢśņŚ¼ ĒؼņäØņŗżĻ│╝ ļåŹņČĢņŗżņØś ņ┤Ø ļČĆĒö╝ļź╝ Ļ│ĀņĀĢĒĢśĻ│Ā ļČĆĒö╝ļ╣äļź╝ ņĪ░ņĀłĒĢ£ Ļ▓░Ļ│╝, ļČĆĒö╝ļ╣ä(VD/VC) 7/1 ņØ┤ņāüņŚÉņä£ļŖö ļ¼╝ņØś Ēł¼Ļ│╝ ņåŹļÅäĻ░Ć ņŚ╝ņØś Ēł¼Ļ│╝ ņåŹļÅäļ│┤ļŗż ļ╣©ļØ╝ņĀĖ ļ”¼ĒŖ¼ņØś ļåŹņČĢņ£©ņØ┤ ņśżĒ׳ļĀż Ļ░ÉņåīĒĢśņśĆļŗż. ļ”¼ĒŖ¼ņØś ļåŹņČĢņ£©Ļ│╝ ĒÅēĻĘĀ ņ£Āļ¤ēņØ┤ ļåÆĻ│Ā ņŚÉļäłņ¦Ć ņåīļ╣äļ¤ēņØĆ ļé«ņØĆ ļČĆĒö╝ļ╣ä 3/1 ņĪ░Ļ▒┤ņØ┤ Ļ░Ćņן ĒÜ©ņ£©ņĀüņØ┤ļ®░, ņØ┤ Ļ▓ĮņÜ░ 5.3 g/LņØś ļåŹņČĢļÉ£ ļ”¼ĒŖ¼ņÜ®ņĢĪ(ļåŹņČĢņ£© : 160.61%)ņØä ĒÜīņłśĒĢĀ ņłś ņ׳ņŚłļŗż.
Acknowledgmentsļ│Ė ņŚ░ĻĄ¼ļŖö 2019ļģäļÅä ņé░ņŚģĒåĄņāüņ×ÉņøÉļČĆņØś ņ×¼ņøÉņ£╝ļĪ£ ĒĢ£ĻĄŁņŚÉļäłņ¦ĆĻĖ░ņłĀĒÅēĻ░ĆņøÉ(KETEP)ņØś ņ¦ĆņøÉņØä ļ░øņĢä ņłśĒ¢ēĒĢ£ ņŚ░ĻĄ¼Ļ│╝ņĀ£(No. 20185210100050)ņØ┤ļ®░, ņØ┤ņŚÉ Ļ░Éņé¼ļō£ļ”Įļŗłļŗż.
Fig.┬Ā3.Determination of the limiting current density by plotting : current density vs. applied voltage. 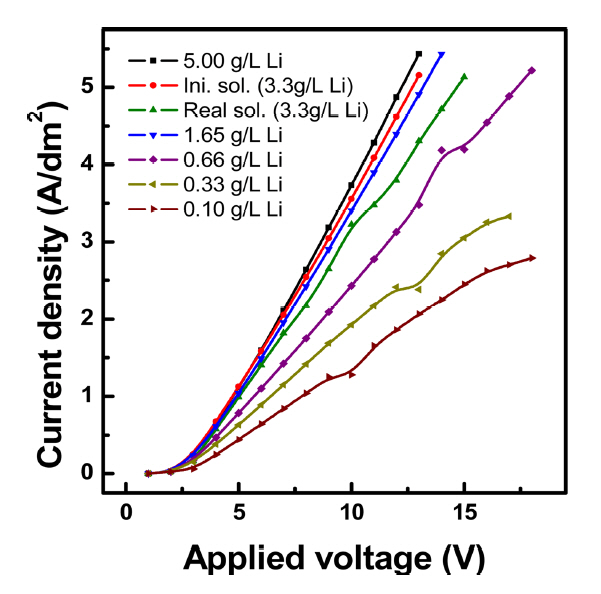
Fig.┬Ā4.Effect of applied voltage on the electrical conductivity(D : Dilute tank, C : Concentrate tank). 
Fig.┬Ā7.Effect of volume ratio and applied voltage on the (a) energy consumption and (b) average flux. 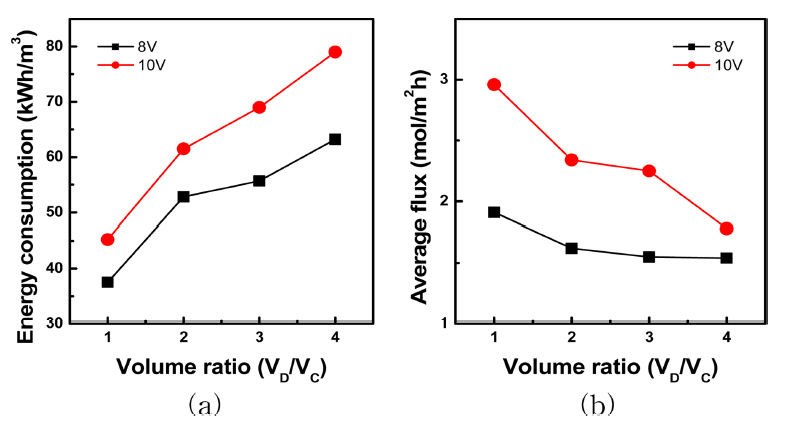
Fig.┬Ā10.Effect of volume ratio and applied voltage on the (a) energy consumption and (b) average flux. 
Table┬Ā1.Specifications of Electro Dialyzer Table┬Ā2.Characteristics of ion exchange membrane (NEOSEPTA) Table┬Ā3.Composition of Li-containing solution used in study (Unit : g/L)
Table┬Ā4.Composition of lithium containing solution used in study (Unit : g/L)
Table┬Ā5.Final concentration of Li+, Na+, SO42- (Unit : g/L)
Table┬Ā6.Effect of applied voltage on the energy consumption and average flux
Table┬Ā7.Final concentration of Li+, Na+, SO42- (Unit : g/L) REFERENCES1. H. W. Yang, J. H. Lee, S. C. Jung, S. T. Myung, W. S. Kang, and S. J. Kim, Korean J. Met. Mater. 54, 780 (2016).
2. Y. M. Yang, C. Loka, D. P. Kim, S. Y. Joo, S. W. Moon, Y. S. Choi, J. H. Park, and K. S. Lee, Met. Mater. Int. 23, 610 (2017).
6. Z. Y. Guo, Z. Y. Ji, Q. B. Chen, J. Liu, Y. Y. Zhao, F. Li, Z. Y. Liu, and J. S. Yuan, J. Clean. Prod. 193, 338 (2018).
7. J. K. Lee, S. G. Jeong, S. J. Koo, S. Y. Kim, and C. S. Ju, Korean Chem. Eng. Res. 51, 53 (2013).
8. A. Umeno, Y. Miyai, N. Takagi, R. Chitraker, K. Sakane, and K. Ooi, Ind. Eng. Chem. Res. 41, 4281 (2002).
9. T. G. Ryu, J. H. Shin, S. M. Ghoreishian, K. S. Chung, and Y. S. Huh, Hydrometallurgy. 184, 22 (2019).
10. J. E. Lee, MasterŌĆÖs Degree Thesis. 9ŌĆō10, Daejin University, Pocheon (2019).
12. J. W. Ahn, H. J. Ahn, S. H. Son, and K. W. Lee, J. Korean Inst. Resources Recycling. 21, 58 (2012).
13. J. K. Lee, S. G. Jeong, S. J. Koo, S. Y. Kim, and C. S. Ju, Korean Chem. Eng. Res. 51, 53 (2013).
14. H. J. Ahn, J. W. Ahn, K. W. Lee, and H. T. Son, J. Korean Inst. Resources Recycling. 23, 21 (2014).
15. H. J. Ahn, MasterŌĆÖs degree thesis. 61ŌĆō62, Daejin University, Pocheon (2014).
16. S. H. Kim and Ph. D. thesis, Ph. D. thesis. 25ŌĆō27, Dankook University, Seoul (2000).
18. Y. H. Jung, S. H. Kang, and Y. K. Chang, Theories and Applications of Chemical Engineering. 7, 1341 (2001).
19. A. M. Peers, Discuss. Faraday Soc. 21, 124 (1956).
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||