AZ31 마그네슘 합금의 플라즈마전해 산화막 두께 성장에 따른 내식특성
Corrosion Characteristics of Plasma Electrolytic Oxidation Treated AZ31 Magnesium Alloy with an Increase of the Coating Thickness
Article information
Trans Abstract
The growth of the PEO coating with processing time on an AZ31B magnesium alloy in a dilute alkaline electrolyte containing silicate and the corrosion characteristics according to its thickness were investigated. The oxide film grew a porous outer layer mainly consisting of silicate with the spark discharge phenomenon from the beginning of the reaction and reached a certain limit thickness later in the reaction. This reaction was followed by the inner layer, mainly consisting of MgO, growing rapidly and densifying. Based on the results of the potentiodynamic polarization and chronoamperometric test, it was found that within 1 minute of the processing time, due to the contribution of the dielectric layer and MgF2 phase layer formed at the interface between the oxide and the substrate, the corrosion resistance was relatively high, but its stability against corrosion was not enough. Moreover, when the thickness of the oxide coating was grown mainly with the silicate outer layer, the increase in the pore size, which acts as a channel of spark discharge, was the leading cause of the decrease in the corrosion resistance. The superior corrosion resistance and the stability of the PEO coating in the later reaction time of the processing are due to the growth and densification of the inner layer of MgO.
1. 서 론
마그네슘은 알루미늄, 티타늄 등과 함께 대표적인 경량금속으로서 지속적인 개발에 따른 산업적 적용 확대 및 시장 확대 가능성이 높게 거론되고 있는 재료이다[1,2]. 그러나 마그네슘과 그 합금들은 낮은 내식성으로 인해 실용소재로서의 제약이 따른다. 표면특성을 보완하기 위한 방법으로 DOW17법과 HAE법 등의 아노다이징 표면처리를 들 수 있지만 내식성과 기계적 물성면에서 부족한 측면이 많은 것이 사실이다 [3,4].
최근 2000년대 들어 플라즈마전해 반응을 이용한 이른바 플라즈마전해산화(plasma electrolytic oxidation, PEO) 방법이 개발되었고, 마그네슘을 비롯한 경량금속 합금의 새로운 양극산화 기술로 주목을 받아오고 있다. PEO는 전해액 중에서 고전압 인가에 따라 발생하는 스파크(spark) 방전현상 및 플라즈마분위기를 이용해 산화막을 형성하는 것으로 기존의 여타 아노다이징에 비해 크게 향상된 내식성과 월등히 높은 경도의 피막을 100 μm 이상으로 성장시킬 수 있다. 그동안 비교적 짧은 기간에도 불구하고 Keronite, Tagnite, Magoxide-coating 등의 상용 기술이 개발되었고, 플라즈마전해와 관련한 원리, 전해액 및 전류 조건, 합금의 종류, 후처리 등 다양한 연구들이 활발히 이루어지고 있다 [5-9].
플라즈마전해 과정에서의 전류는 주로 전기화학적 반응에 의해 피막을 형성시키는 이온전류(ionic current)와 전기 방전 현상에 따른 전자전류(electron current)의 단독 혹은 혼합 기여로 설명된다 [10-12]. 이러한 전류들의 기여는 전형적인 전압변화 거동을 나타내게 되는데, 마그네슘합금의 PEO과정에서 전압변화 거동과 관련해 Guo 등은 처리 시간에 따라 전압 거동이 2번의 굴곡점을 포함하는 3개의 영역으로 나타남을 보였다 [13,14]. 이들은 또한 PEO과정에서 기공의 구조가 처리시간에 따라 그 수가 줄어드는 동시에 크기는 증가하는 경향을 보고하는 한편, forsterite의 Mg2SiO4와 MgO가 산화막을 구성하는 주요 상이 된다고 하였다. Chang 등도 마그네슘 합금의 PEO과정에서 인가전류에 따라 동일한 3단계의 전압변화 거동에서 첫 번째와 두 번째 단계의 전압상승 속도에 차이가 나타남을 보였으며, 외부로 성장한 피막두께와 내부로의 두께 사이의 비율이 처리시간에 따라 6:4에서 4:6 정도로 달라짐을 나타내었다 [15].
다양한 마그네슘 합금 종류에 따른 PEO처리 방전특성들과 형성된 산화막의 두께, 경도, 내식성들이 Arrabal 등의 연구를 통해 보고된 바 있다 [16]. 또한, Walsh 등은 AZ91 합금에서 PEO가 산화막내 기공이 상대적으로 적은 구조를 형성하기 때문에 DC 아노다이징에 비해 염수분무에 대한 내식성이 약 3배로 길어지는 것으로 설명하였다 [17]. Barchiche 등은 전해액의 KOH농도, 아노다이징 시간 및 전류밀도가 AZ91D 합금의 플라즈마전해 산화막의 내식성에 미치는 영향을 양분극과 음분극과 함께 시간대전류법(chronoamperometry) 실험을 통해 조사하였으며, PEO 산화막의 보호특성이 기공률에 크게 의존하는 것으로 보고하였다 [18]. Ma 등도 AM50합금에 대한 PEO처리시 KOH 농도가 코팅의 내식성에 가장 큰 영향을 미치며, 코팅의 상조성, 두께 및 균일성의 원인으로 내식성 차이가 나타난다고 하였다 [19]. Liang 등은 AM60합금 PEO처리시 KOH 전해액을 기본으로 실리케이트와 인산염의 첨가에 대한 특성 차이를 연구하여, 실리케이트를 첨가한 경우가 상대적으로 경도가 높고 내마모성이 우수하다고 하였다. 동전위분극시험을 통한 내식성 비교에서 두 경우 모두 PEO처리하지 않은 상태에 비해 향상된 내식성을 나타내었는데, 실리케이트를 첨가한 경우가 인산염을 첨가한 경우보다도 우수하게 나타났다 [20]. Zhang 등의 알루미늄-스테인리스스틸-마그네슘의 갈바닉 부식실험에서 마그네슘의 PEO처리 두께 증가에 따라 전체 부식속도는 늦어지며, 부식에 의한 무게 감소가 최대 100배까지 나타난 바 있다 [21].
이처럼 마그네슘 합금의 PEO처리와 관련한 많은 연구들이 이루어져 왔음에도 불구하고, 산화막의 두께 성장과 이와 관련한 내식성 등 특성에 대해서는 여전히 구체적이고 명확하게 제시되지 못한 부분들이 있다. 본 연구에서는 AZ31B 마그네슘 합금을 대상으로 기본적인 KOH-실리케이트 전해액 중에서 PEO처리시 시간에 따른 산화막의 성장거동을 면밀히 조사함과 아울러 두께 성장에 따른 내식성의 변화를 전기화학적 방법을 통해 밝히고자 하였다.
2. 실험 방법
연구에는 3 mm 두께의 판재 AZ31B 마그네슘 합금을 사용하였고, PEO 처리면적은 20 cm2으로 하였다. 시편의 전처리로 #600의 연마포를 이용해 표면을 연마한 다음 중성 용액에서 세척하고 공기로 블로잉 건조하였다. 플라즈마전해에 사용된 전해액은 1.5 g/L KOH + 5 g/L KF + 8 g/L Na2O(SiO2)x·xH2O의 조성을 갖는 희박(dilute)농도의 알칼리 수용액으로 하였다. 전해장치는 10 리터급 전해조와 냉각장치 및 정류기로 구성하였으며, 상대전극은 2 mm 두께의 304형 스테인리스 스틸 판으로 시편처리면적의 20배 이상의 면적을 갖도록 하였다. 전해에는 380 V, 60 Hz, 3상 교류의 입력 전원을 갖는 정류기가 사용되었으며, 출력전류는 정현파의 단상 교류로서 피크값을 기준으로 1,000 mA/cm2 의 조건으로 인가 하였다. 또한 PEO처리 과정에서의 실제 전류 출력은 발생하는 플라즈마전류를 제어 프로그램에 의해 보상하여 변동되는 것으로 하였다. 전해액의 온도는 처리개시 전 10 °C로 하였으며, 처리과정에서 전극가열에 의한 온도상승을 20 °C 이내에서 유지되도록 하였다.
PEO 산화막 성장거동을 고찰하기 위해 매 1분 단위로 시간을 증가시키며, 최대 10분까지 처리를 실시하였다. 또한 초기 변화를 확인하기 위해 5초와 20초 동안 처리한 샘플을 추가하여 준비하였다. 전자현미경(Hitachi, SU5000) 관찰을 통해 처리 시간에 따른 PEO 산화막의 단면 및 평면 이미지를 확인함과 아울러 산화막의 두께를 측정하였다. 또한 시간 변화에 따른 PEO 산화막의 원소 분포를 알아보기 위해 EDS(HORIBA, EMAX)를 이용해 조사하여 나타내었다.
PEO 산화막에 대해 X선 회절분석으로 구성 상(phase)분석을 실시하였다. 이때 산화막의 외부 표면과 내부면을 구별하여 분석하였는데, 내부면은 산화막의 두께가 약 40 μm가 남을 때 까지 연마하여 분석에 사용하였다. 회절분석조건은 Cu Kα radiation (λ=0.15406)을 사용하여 2θ = 10° ~ 80°, 스텝 크기 0.05°로 하였다.
한편 최대 10분까지 PEO 처리과정에서 전압 및 전류변화 거동을 측정(Keithley, DMM6500 / Fluke, DMM 289)하였고, 형성된 산화막들의 단면조직에 대해 마이크로비커스 경도(Mitutoyo, HM-220)를 측정하여 기본적인 기계적 물성을 조사하였다. 경도측정은 피막의 두께와 압흔의 길이를 고려하여 0.245 N의 하중으로 실시하였으며, 산화막의 각 부위에 대해 9군데씩 측정 후 그 평균값을 산정하였다.
처리시간에 따른 내식성 차이를 동전위분극시험(potentiodynamic polarization)을 통해 비교 분석하였으며, 전위차계(potentiostat) (AMETEK, PARSTAT4000)와 1 cm2의 시편 노출 면적을 갖는 Flat cell (PARC model. K0235)이 사용되었다. 시험은 3.5 wt% NaCl용액에서 실시하였으며, 전해액에 대한 별도의 탈기처리 없이 대기포화 상태로 실온을 유지하였다. 전위 범위 및 주사속도는 각각 –1.8에서 –0.25 V (vs. Ag/AgCl), 5 mV/sec.로 하였다. 또한 시간대전류법을 통해 피팅(pitting)거동과 산화막의 안정성을 함께 평가하였다. 3.5 wt% NaCl 용액을 이용해 Ecorr + 200 mV 의 조건으로 과전압을 인가하였으며, 시간에 따른 전류변화를 측정하였다.
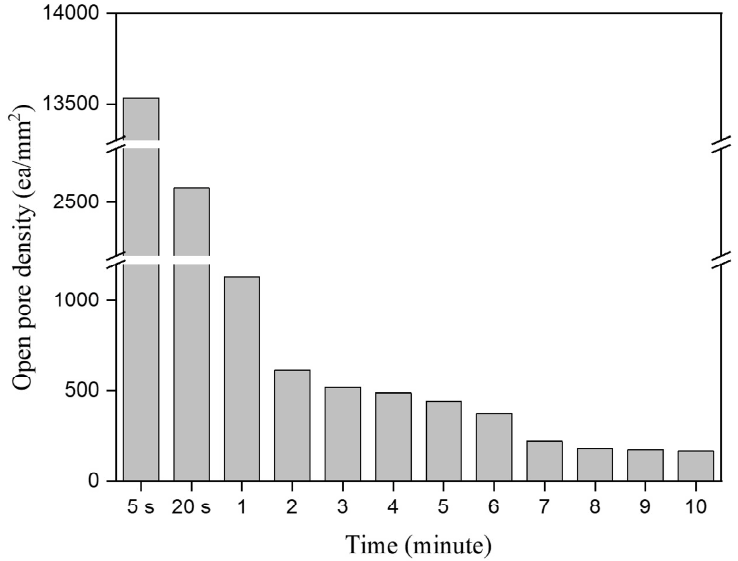
PEO 산화막의 기공이 내식성에 미치는 영향을 고찰하기 위해 각 처리 시간에 따른 open pore(defect) density를 측정하였다. 측정은 3.5 wt% NaCl 용액에 1 시간 침적 후 60 g/L CH3COOH + 5 g/L CuSO4·5H2O + 15 g/L ZnCl2·7H2O 용액에 1 분간 침적 처리하여 순수로 세척한 다음 건조시켜 표면으로 점상 돌출된 부식생성물의 수를 200배율의 광학현미경 관찰을 통해 세는 방법으로 이루어졌다 [22,23].
3. 결과 및 고찰
그림 1은 PEO처리 시간에 따라 형성되는 산화막의 단면 이미지를 나타낸 것이다. 모든 단면 이미지에서 outer layer와 inner layer로 구별할 수 있는 2개의 층을 이루는 전형적인 PEO 산화막을 보이고 있다. (a) 5초 및 (b) 20초에서는 약 5 μm 이내의 두께를 갖는 얇은 막을 형성하고 있으며, 모재와의 계면에 1 μm 미만의 연속적인 층과 함께 다공성의 외부 구조를 나타낸다. 또한, (c) 1분 이후 (h) 6분에 이르기까지 약 10 ~ 35 μm 두께로 피막이 두꺼워짐을 보이고 있다. 이들 6분 이내의 경우들에서 outer layer는 큰 기공이 많은 불규칙적인 구조를 가지고, inner layer 역시 비교적 작고 많은 기공의 다공성 구조를 가진 것으로 확인된다. 처리시간 (i) 7분 이상의 경우들에서는 시간 증가에 따라 inner layer가 두껍게 성장함을 알 수 있는데, 내부 기공이 감소되며 치밀한 구조로 나타나며 치밀해진 inner layer는 다수의 크랙을 포함하는 것이 관찰된다. Outer layer에서의 크랙은 (g) 5분 이상의 모든 경우들에서 나타나고 있다. 한편, 최대 (l) 10분까지 처리하여 형성된 피막의 전체 두께는 약 90 μm에 이르는 것으로 나타났다.
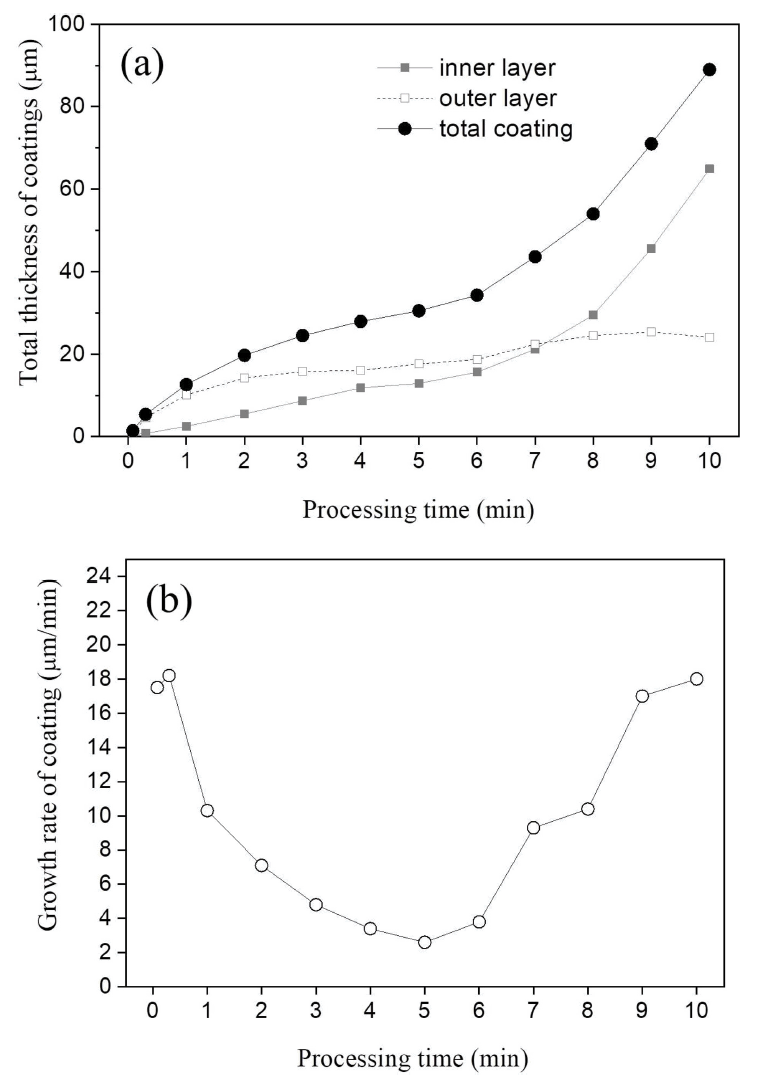
단면 이미지로부터 이미지 분석 소프트웨어를 이용해 각 처리시간에 따른 산화막의 평균두께를 산정하였으며, 전체 산화막의 두께 변화를 그림 2(a)에 나타내었다. 전체적으로 반응 초기와 더불어 6분 이후 급격한 두께 증가가 나타나는 역 ‘S’자 형태의 거동을 보이고 있다. 그림 1에서 나타난 inner layer와 outer layer의 평균적인 두께를 함께 나타내었는데, 6분 이내까지는 outer layer가 inner layer에 비해 더 큰 비율을 보이며, 8분 이후 산화막에서는 inner layer가 전체 두께에서 차지하는 비율이 보다 높아지며 그 두께 증가가 현저하게 나타나고 있음을 알 수 있다. 반면 outer layer는 처리시간 2분까지 약 15 μm 두께로 빠르게 형성된 다음 최종 10분에 이르기까지 약 25 μm 이내의 두께로 증가 폭이 작다.
또한, 이를 산화막의 성장속도로 환산하여 그림 2(b)에 함께 나타내었다. 초기 1분 이내에서 분당 10 μm 이상의 속도로 빠르게 성장함을 보이고 있는데, 5초의 경우 정류기로부터의 전류상승 시간이 포함되며, 플라즈마 혹은 방전현상과 무관하게 전기화학적 반응에 의해 실리케이트 등 산화막이 빠르게 형성되는 것으로 사료된다. 20초의 경우 마이크로스파크(micro-spark) 발생이 수반되기는 하지만 앞 단계에서 형성된 산화막의 지속적인 두께 성장에 따른 것으로 판단된다.
이후 전체 처리시간의 절반에 해당하는 5분에 이르기까지 성장속도는 점차 감소하여 약 2 μm/min에 이르게 된다. 6분 이후 후반부가 되면서 다시 빠르게 증가하여 10 μm/min 이상으로 최대 약 18 μm/min의 성장 속도를 보이게 된다. 이처럼 성장 속도는 PEO처리 시간에 따라 초기와 후기로 갈수록 빨라지고 중간단계에서 느린 형태인 ‘U’자형 변화 거동을 나타낸다.
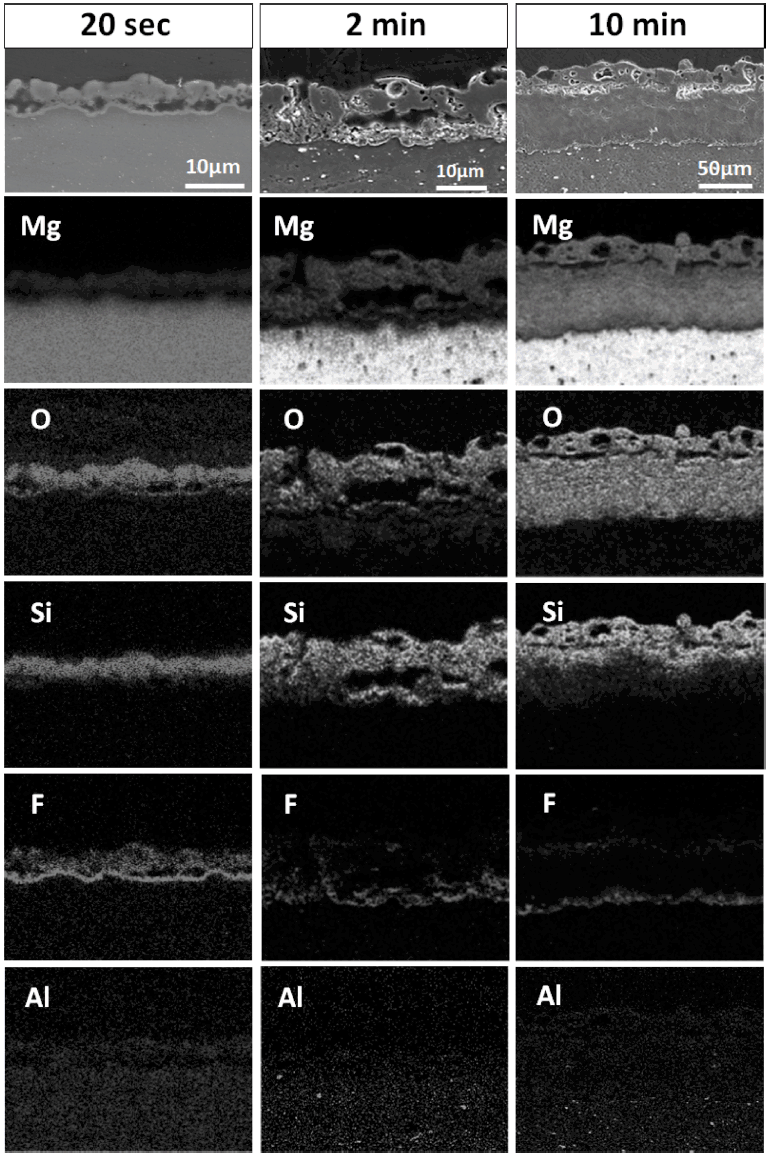
한편, 그림 3에 EDS(energy dispersive spectroscopy)를 이용해 조사한 시간 변화에 따른 PEO 산화막의 원소 분포를 나타내었다. 단면 형상의 특징을 반영하여 극초기의 20초를 비롯해 처리시간의 전반부에 해당하는 2분 및 최종 10분에 대한 결과를 나타내었으며, 원소는 전해액의 성분 등을 고려하여 Mg, O, Si, F, Al의 분포를 나타낸 것이다. 먼저 산소와 마그네슘의 경우 모든 경우의 코팅층 전체에서 분포하며, 이는 outer layer와 inner layer 모두 기본적으로 산화물 구조임을 시사하는 결과이다. 실리콘의 경우 모든 outer layer에 집중적으로 나타나는 것으로 확인되고 있어, outer layer는 실리케이트계 상을 형성하고 있는 것으로 추정해 볼 수 있다. 또한, inner layer에 있어 마그네슘의 분포와 달리 실리콘은 분포가 적으며, 이러한 분포는 10분 처리한 경우에서 현저히 나타나고 있다. 뿐만 아니라, 20초에 나타난 모재 계면의 연속적인 층에는 불소화합물이 집중적으로 형성되어 있음을 확인할 수 있는데, 이는 전해액 중 KF에 의해 형성된 MgF2 화합물로 추정된다. 2분 및 10분 처리한 경우에서의 불소 분포가 불연속적으로 나타나는 것으로부터 MgF2 는 초기 계면에서 형성된 후 코팅층 성장에 따라 산화막 내부로 분산되어 가는 것으로 판단된다. 또한 처리시간 20초 이하와 같은 초기의 경우 2분 이상의 경우와는 달리 MgF2 와 순수 실리케이트로 코팅층이 구성되는 것으로 사료된다. Al의 경우에는 산화막내 가시적인 분포가 확인되지 않았다.
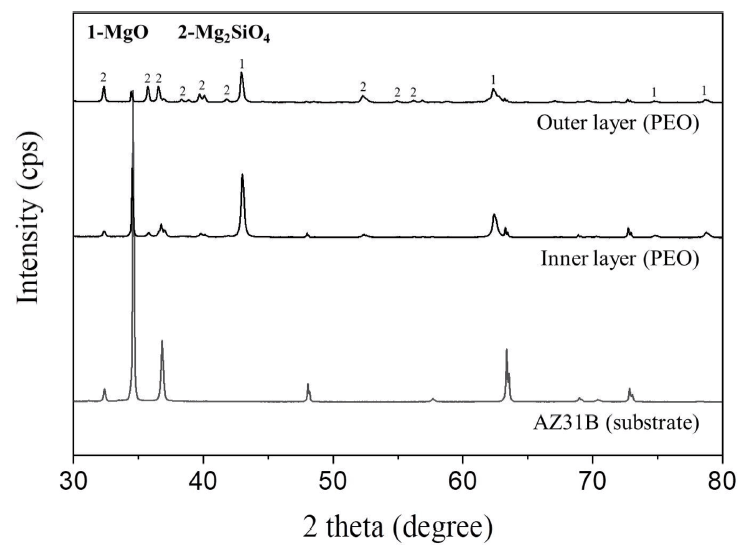
PEO 산화막의 구성 성분을 보다 명확히 확인하기 위해 10분간 처리한 코팅층에 대해 outer layer와 inner layer를 구별하여 X선 회절분석을 실시하였으며, 그 결과를 그림 4에 나타내었다. 모재인 AZ31B의 회절패턴을 함께 나타내었는데, outer layer와 inner layer 모두에서 34.6°, 36.8°, 48.1°, 63.4°, 72.9°의 관련 피크가 관찰된다. 이는 다공성의 산화막 구조에 따른 영향으로 추정되며, 평균 40 μm 정도의 두께로 연마하여 측정한 inner layer에서 보다 뚜렷이 확인된다. 회절패턴에서 주로 MgO (2θ=43.0°, 62.4°, 74.9°, 78.8°)와 Mg2SiO4 (2θ=32.3°, 35.7°, 36.5°, 39.7°, 40.0°, 41.8°, 52.3°)의 피크들이 나타나는데, outer layer에는 이 두 종류의 피크들이 모두 나타난다. 그러나 inner layer에서는 일부 Mg2SiO4의 피크들이 나타나기는 하지만 상대적으로 강한 MgO의 피크를 보이고 있다. 이들 결과로부터 outer layer는 Mg2SiO4의 실리케이트를 주로 하여 MgO를 포함하는 혼합 상을 이루고 있으며, inner layer는 이와는 반대로 MgO를 대부분으로 하여 소량의 실리케이트상을 포함하는 것으로 판단된다. 또한 이는 앞서 EDS를 이용한 원소분포에서 나타난 결과와도 일치하는 결과이다. 한편, X선 회절분석 결과에서는 가시적인 MgF2의 피크는 관찰되지 않았는데, 이는 분석이 진행되는 표면부에 MgF2의 함량이 사실상 미미하기 때문으로 사료된다.
PEO처리 시간에 따라 형성되는 산화막의 표면 이미지를 그림 5에 나타내었다. 모든 시간에 대해 표면 전체에 걸쳐 다량의 기공 구조가 관찰된다. (a) 5초 및 (b) 20초에서는 수십 ~수백 nm의 기공과 수백 nm ~ 1 μm 이내 크기의 기공들이 각각 나타난다. (C) 1분 이후 (g) 5분에 이르기까지 시간의 증가에 따라 기공들이 불규칙적인 형상으로 그 크기가 커지는 것을 알 수 있으며, 이 사이에 기공의 수는 감소하는 양상을 나타내고 있다. (h) 6분 이후 이미지들에서도 여전히 수 ~수십 μm의 크기를 갖는 다수의 기공들이 관찰되나 처리시간에 따라 현저한 크기와 수의 증감은 나타나지 않는다. 또한, 5분 이후의 형상들에서는 PEO의 전형적인 ‘volcano-like’형태의 표면들이 잘 나타나고 있으며, 이들 기공들은 PEO과정에서 스파크 방전의 채널 역할을 통해 나타나는 것으로 알려져 있다.
그림 6에 PEO 진행 과정에서 실제 전극에 발생하는 (a) 전압 및 (b) 전류 변화를 측정한 결과를 나타내었다. 또한 (c)에는 초기 1분 이내의 변화를 확대하여 보다 자세히 나타내었다. 먼저 전압변화와 관련해 (I 구간) 최초 약 7초 이내에서 약 220 V (rms AC)까지 급상승한 후 (II 구간) 변곡점을 나타내며 상승속도가 다소 완화된다. 약 30초까지 직선적으로 상승하여 약 280 V 정도에 도달하게 되는데, (III 구간) 두 번째 변곡점 이후 일정시간 비교적 일정한 전압을 유지하면서 약 270 V 로 약간씩 낮아지는 모습을 보이다가 (IV 구간) 7분경에 다시 상승하여 최종 10분 종료직전 약 290 V에까지 이르는 것으로 나타난다. 전류의 경우 초기 급상승 후 다소 감소하여 일정시간 유지되고, 3분 이후 추가로 감소한 다음 지속적인 증가를 소폭 보이다가 7분에 이르러 최종까지 더욱 증가하는 현상을 나타내고 있다. 이러한 전류의 변화는 전압의 변화를 4개의 구간으로 나타낸 시점과 거의 동일하다. PEO처리 과정에서 전류 및 전압의 변화 거동은 산화막의 형성 및 성장과 밀접한 관련이 있으며, 본 실험결과에서 I ~ III 구간은 기존의 연구들에서 설명된 3단계 거동과 동일한 것으로 판단된다. I 구간에서는 표면에서 이온전류(ionic current)만으로 스파크가 발생하지 않은 채 가스만 지속적으로 생성되며 얇은 산화막이 형성되는 구간이다. II 구간은 절연 파괴에 따라 표면 전반에 걸쳐 마이크로 스파크가 발생하는데, 전자전류(electron current)의 기여가 나타난다. 이러한 전자전류는 이온전류와 달리 산화막의 형성과 무관하기 때문에 전압의 상승을 유발하지 않는 것으로 알려지고 있다. 전체 전류에서 전자전류가 차지하는 비율의 증가에 따라 II 구간이 끝나는 지점인 임계 전압(critical voltage)에서 전압의 기울기가 0에 가까워지며 III 구역으로 들어서게 된다. III 구간에서는 II 구간보다 점차 스파크의 수는 감소하지만 그 크기는 커지게 된다 [14]. 전류변화와 관련해서 본 실험에서 나타난 II, III 구간에서의 전류감소는 방전현상에 의한 전류, 즉 전자전류가 정류기를 통해 인가되는 전류를 상쇄시키는 역할을 하는 것으로 사료된다. 기존의 연구들과 달리 본 연구에서는 처리시간 약 7분 이후 반응 후반기 부분에 전압과 전류가 다시 상승하는 IV 구간을 추가로 구분하였다. 몇몇 기존의 연구들에서 4개의 단계로 구분하여 설명한 바 있으나, 이들 대부분이 II구간과 III구간 사이에 전압 거동 기울기가 조건별로 다소 달라지는 것을 구분한 것으로 본 연구에서의 현상과는 차이가 많다. IV 구간에서의 전압 및 전류의 상승은 그림 1 및 3에서 나타낸 산화막 형성 및 성장 결과로부터 하부 inner layer의 MgO 산화막과 관련한 것으로 유추해 볼 수 있다. 반응 후반부의 전압 및 전류 상승과 관련해 Timoshenko를 비롯한 Gebarowski 등의 연구로부터 높아진 교류전원의 negative phase 전압에 의해 형성된 대량의 수소막이 절연저항 역할을 함으로써 큰 규모의 전기화학적 반응을 유발하고 이에 따른 전류·전압의 상승 및 빠른 MgO 산화막 성장을 유발하는 것으로 사료된다 [24,25].
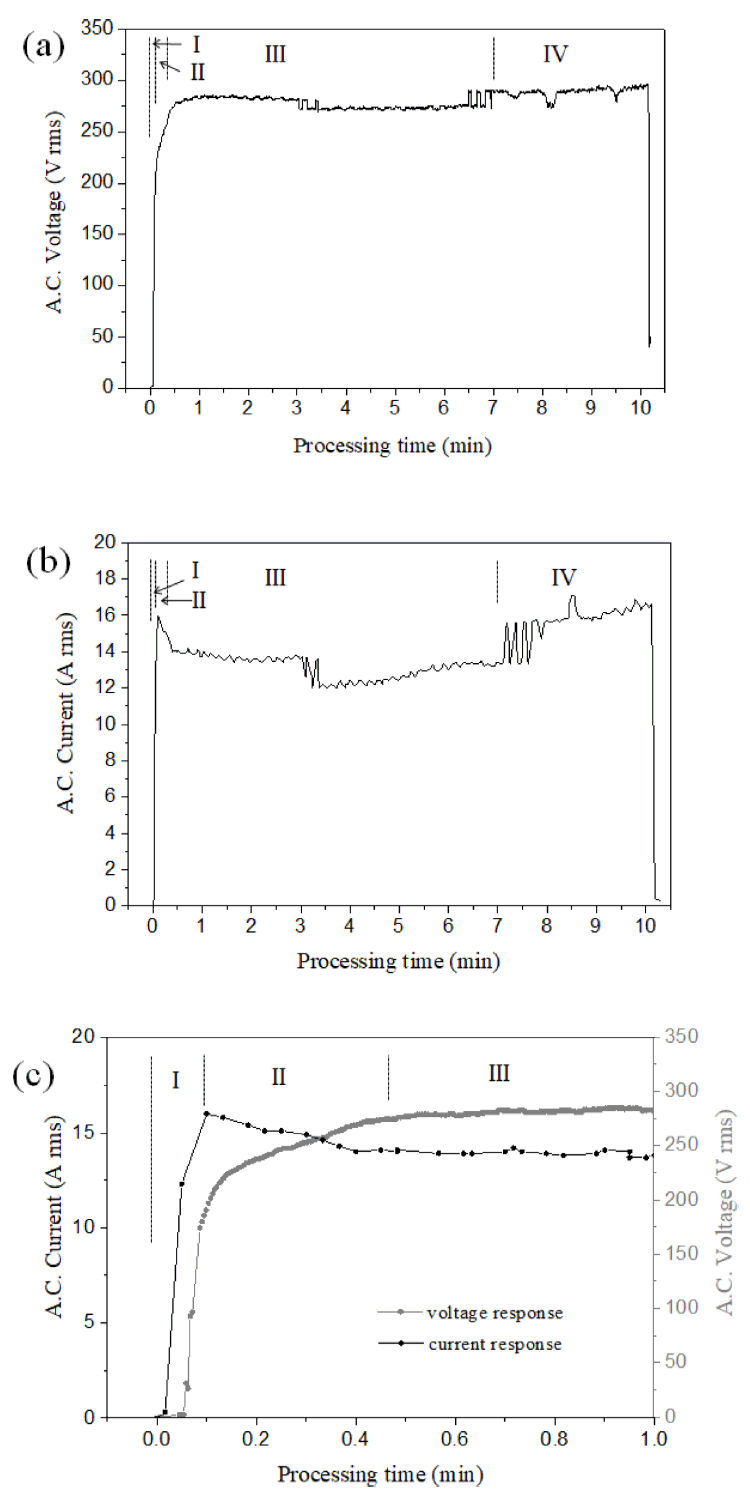
(a) Voltage and (b) current responses during PEO process of AZ31B, (c) zoomed-in view of initial variation within 1minute.
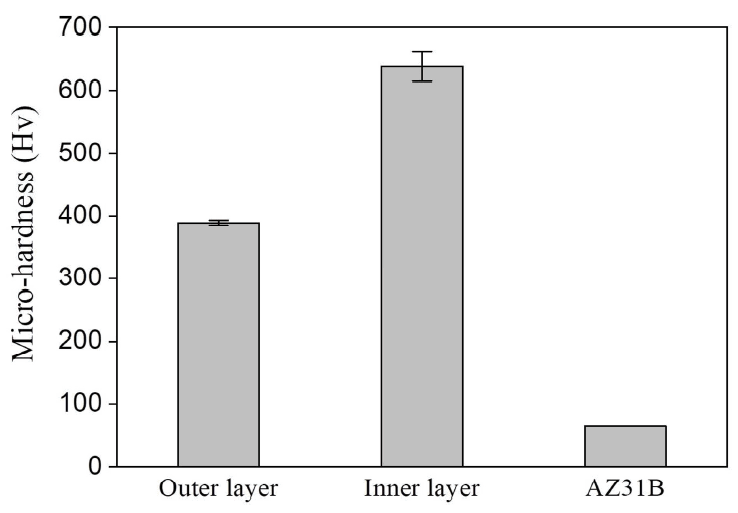
그림 7는 PEO 산화막과 모재 AZ31B의 경도를 측정한 그래프이다. Outer layer와 inner layer의 구분이 가능한 PEO 공정 8분부터 10분 까지 처리한 경우들에 대해 측정한 결과 시간의 증가와는 무관하게 outer layer와 inner layer는 각각 평균 390 Hv와 640 Hv의 경도값을 나타내는 것으로 확인되었다. 이는 모재인 AZ31B의 경도값이 65 Hv 정도이고, 종래의 DOW17 아노다이징 피막의 경도가 약 250 Hv 수준임을 감안할 때 PEO처리를 통해 매우 높은 수준의 기계적 표면물성 확보가 가능함을 나타낸다.
각 처리시간에 따른 PEO 코팅이 내식성에 미치는 영향을 알아보기 위해 3.5 wt% NaCl 용액에서 실시한 동전위분극시험 결과를 그림 8에 나타내었다. 곡선들의 가독성을 돕기 위해 처리시간 5분 이내와 이상으로 나누어 (a)와 (b)에 각각 도시하였는데, PEO처리를 하지않은 AZ31B 모재와 5분 처리한 경우를 함께 나타내었다. 또한, 분극시험 결과로부터 부식전위(Ecorr)와 부식전류밀도(Icorr), 분극저항(Rp) 값을 산정하여 표 1에 나타내었다. 이 때, 부식전위 ±100 mV 범위내에서 외삽하여 접선의 교점으로부터 부식전류밀도를 결정하였다. 또한 접선의 기울기로부터 애노딕 및 캐소딕 타펠 상수 βa 및 βc 를 구하고 식 (1)에 표현된 Stern-Geary식을 이용해 분극저항값(Rp)을 산정하였다.
5분이내에서 부식전위는 -1.50 ~ -1.48 V 사이의 값을 나타내며 초기에 해당하는 1분이내의 경우들에서 약 17 kΩ 이상의 상대적으로 높은 분극저항 값을 갖는 것으로 나타났다. 반면 2 ~ 5분 사이의 경우, 1분 이내의 경우들 보다 높은 부식전류밀도 및 낮은 분극저항을 나타낸다. 5분 이내에서는 전반적으로 처리시간의 증가에 따라 부식전류밀도는 증가하고, 분극저항은 감소하며, 부식전위는 소폭 상승하는 경향을 보이고 있다. 이러한 현상은 1분 이내, 특히 5초와 20초의 경우에서 반응초기 형성되는 절연층(dielectric layer)과 더불어 모재 계면에 집중되는 층을 이루는 MgF2의 기여에 따른 것으로 사료된다. 반면에 2분 이상이 되면 그림 1(d) ~ (g)와 5(d) ~ (g)에 나타낸 바와 같이 기공의 크기가 증가하는 현상에 따른 것으로 추정된다. 기존의 연구들에서도 PEO코팅의 기공이 내식성에 주요인자가 되는 것이 보고된 바 있다 [17,18]. 또한 그림 3에서 나타난 바와 같이 MgF2는 산화막 성장에 따라 점차 흩어지며 계면에 집중된 층을 이루지 못함으로써 내식성에 대한 기여가 점차 줄어드는 것으로 사료된다. 따라서 이때의 내식성은 inner layer의 기여가 낮고, 실리케이트로 구성되는 outer layer의 방전채널인 기공의 크기에 의존하는 것으로 판단된다. 한편, 5초와 20초의 경우에는 각각 -1.21 및 -0.71 V의 양분극 상태에서 전류밀도가 급증하는 형태를 나타내는데 이는 초기에 형성된 얇은 절연막이 높은 과전압을 견디지 못하고 파괴되는데 따른 것으로, 이때의 PEO 코팅층은 보호피막으로서 충분히 견고하지 못하다는 점을 시사한다. (b)의 처리시간 6분 이상의 경우에도 7분 이내와 8분 이상으로 구별되는 차이를 보이고 있는데, 7분 이내의 경우 5분의 경우와 유사한 거동을 보이고 있으며, -1.44 및 -1.43 V의 부식전위값을 나타낸다. 8 ~ 10분의 경우들에서는 -1.32 ~ -1.29 V의 부식전위로 높은 값을 나타내며, 부식전류밀도가 크게 줄어드는 것으로 나타나고 있다. 분극저항 또한 20 kΩ 이상으로 크게 증가하는 것을 나타내었다. 이는 그림 1(j) ~ (l)에 보이는 것과 같이 MgO를 주상으로 하는 inner layer의 현저한 성장과 치밀화에 의해 급격한 내식성 향상이 나타나는 것으로 판단된다. 다만, 8분과 9분의 경우 높은 과전압조건에서 전류밀도가 급증하는 모습을 보이는데, MgO 산화막의 치밀성 혹은 견고성이 처리시간 10분의 경우에 미치지 못하는 것으로 사료된다. 따라서, 최종 10분 처리한 경우가 가장 우수한 내식성을 나타내는 것으로 확인된다. 이상의 분극시험 결과로부터 모든 PEO처리 시간에서 AZ31B 마그네슘합금에 대한 내식성 향상 효과를 기대할 수 있으며, 특히, inner layer를 두껍게 성장시킴으로써 현저한 효과를 얻을 수 있음을 알 수 있다.
한편, AZ31B 소재가 3 wt%의 Al을 포함하고 있음에 따라 그 영향을 생각해 볼 수 있으나, 앞서 EDS 및 XRD 결과들에 산화막내 Al 원소 및 관련 화합물의 유의미한 분포가 확인되지 않음에 따라 PEO 피막 형성과 성장을 비롯해 이후 내식성에 미치는 영향이 극히 미미할 것으로 추정된다.
그림 9은 내식성과 관련하여 PEO 산화막의 안정성을 평가하기 위해 실시한 시간대전류 곡선으로 AZ31B 모재와 더불어 처리시간 20초, 3분, 6분, 8분, 10분에 대해 나타내었다. 결과에서 PEO 처리를 하지 않은 AZ31B 모재의 경우, 매우 빠르게 전류가 증가하여 피크를 나타내고 약 15 mA의 비교적 일정한 한계전류를 나타낸다. 또한, 지속적인 전류 진동을 보이는데, 이는 마그네슘 합금의 표면에서 피팅에 의한 부식이 발생함을 나타내는 것에 따른 것으로 추정된다. 이와는 달리 PEO처리된 경우들에서는 한계전류에 도달하기까지 시간지연이 나타나는데, 20초와 3분, 6분의 경우들에서는 전류증가의 지연현상이 나타나기는 하지만 10분 및 8분의 경우들에 비해 1000초 이내에서 상대적으로 빠르게 전류증가가 나타나고 있다. 10분 및 8분 처리한 경우 전류증가의 지연이 약 3000초 이상이 되는 것으로 확인되며, 특히 10분의 경우에 가장 작은 기울기를 나타낸다. 4000초 이상의 한계전류와 관련해서 3분의 경우 AZ31B 모재와 대등한 수준에 이르고, 20초, 6분, 8분의 경우 이보다 낮은 약 12 mA 정도를 나타난다. 10분의 경우에는 약 6 mA 정도의 가장 낮은 한계전류를 보임으로써 동전위분극 결과 나타난 가장 우수한 내식성과 함께 장시간에 걸친 수식환경에서도 우수한 안정성을 갖는 것을 알 수 있다.
Open pore density를 측정한 결과를 그림 10에 나타내었다. 이는 표면에 나타난 기공 또는 크랙과 같은 결합 중 모재계면까지 연결된 이른바 ‘open pore’를 확인한 것이다. 1분에서 10분까지 PEO처리시간이 증가함에 따라 open pore의 수가 점차 감소하는 경향을 보이며 최종 처리시간 10분의 기공의 수는 171 ea/mm2을 나타내었다. 이는 시간이 증가할수록 우수한 내식성을 나타내었던 분극시험의 결과에 부합하는 것으로, PEO 산화막의 성장에 따라 open pore의 수가 감소하고 그 결과 높은 분극저항과 같은 내식성 향상의 요인이 되는 것으로 판단된다. 한편, 초기인 5초와 20초에서는 각각 13,536 ea/mm2, 2,580 ea/mm2의 open pore로 월등하게 높은 수를 나타내어, 양호한 내식성을 타나내었던 분극시험의 결과에 상반되는 결과를 나타내었다. 이는 아세트산 등으로 이루어진 측정조건의 부식 용액이 보다 가혹한 조건으로 분극시험 결과에서 나타난 부식전위 보다 훨씬 높은 과전압 조건, 즉 그림 8(a)의 분극 시험 결과에서 –0.5 V 이상과 유사한 상태를 유발하는데 따른 것으로 추정되는데, -0.5 V 이상에서 5초와 20초 처리한 경우들이 높은 전류밀도를 보이고 있다.
4. 결 론
AZ31B 마그네슘 합금을 대상으로 KOH-실리케이트 전해액 중에서 PEO처리시 시간에 따른 산화막의 성장거동 및 두께 성장에 따른 내식성의 변화를 조사하여 다음과 같은 결론을 얻었다.
1. PEO 처리를 통해 형성되는 산화막은 반응초기부터 스파크 방전 현상과 함께 실리케이트를 주상으로 하는 다공성의 outer layer를 위주로 성장하다가 반응 후반 일정 한계 두께에 다다르게 되며, 이후 under-layer 방전이 진행되면 MgO를 주상으로 하는 inner layer가 매우 빠른 속도로 두께가 급성장하게 되는 동시에 치밀해진다.
2. PEO 산화막 형성 및 성장과정에서 전류, 전압 변화는 다음의 네 구간으로 구분된다. 반응 극초기 절연막이 형성되며 전압, 전류가 동시에 급상승하는 I 구간, 절연파괴와 함께 전면적인 마이크로 스파크가 발생되며, 전압은 연속적으로 증가하나 전류는 감소하는 II 구간, 크고 안정적인 스파크가 발생하며, 전압 및 전류가 일정해지는 III 구간, 반응후기 국부적인 스파크와 함께 under-layer방전이 발생하며, 전압 및 전류가 다시 상승하는 IV 구간이다. 이들 구간에서 I, IV 구간은 이온전류가 II, III 구간은 전자전류의 기여가 높은 구역에 해당한다.
3. 동전위분극시험을 통한 내식성 분석 결과, 초기 1분 이내에는 형성된 절연막과 모재계면에 집중하여 층을 이루는 MgF2상의 기여로 인해 상대적으로 높은 내식성을 나타내지만, 부식에 대한 안정성이 다소 떨어진다. 실리케이트 outer layer를 위주로 산화막 두께 성장시에는 스파크 방전의 채널 역할을 하는 기공크기 증가가 내식성 감소의 주요 원인이 되며, 반응 후기 우수한 내식성과 산화막의 안정성은 MgO의 inner layer의 성장과 치밀화에 따른 것이다.
Acknowledgements
이 논문은 2019년 국가과학기술연구회 중소기업지원사업으로 지원을 받아 연구되었음.