고전류밀도에서의 탄산칼륨 첨가제의 전해동박 특성에 미치는 영향
Effect of Potassium Carbonate Additives on the Properties of Copper Foils Electroplated at High Current Density
Article information
Trans Abstract
The amount and kind of additives in electrolytes play a very important role on the electroplating of Cu foil, which is used as a cathode materials for secondary batteries. As the use of Cu foil increased, various studies on the electroplated Cu foil are urgently needed. We studied surface characteristics and changes in structural properties due to the addition of inhibitors under electroplating conditions with high current density. The surface layer was observed, to analyze the effect of the amount of potassium carbonate as an inhibitor. When the potassium carbonate was added at 5~25 ppm without any other additives, the initial plating voltage was observed to decrease. To uniformly distribute crystals without agglomeration at the initial stage of electroplating, it is reasonable to add potassium carbonate within the range of 20~25 ppm. There was no significant difference in surface roughness and specific resistance due to the amount of potassium carbonate, when the additives were added complexly. There was an increase in the relative strength of the preferred growth orientation of (220) in a group with 20 ppm potassium carbonate, compared to the group with 10 ppm potassium carbonate. The grain size decreased with the amount of potassium carbonate added with other additives. However, there was no significant difference in tensile strength and elongation (p-value: 0.000). To ensure uniform properties with a combination of 4 kinds of additives it is reasonable to add potassium carbonate in the range of 10~20 ppm.
1. 서 론
최근 들어 전기차 시장이 확장되며 전기차용 배터리 즉 이차전지 시장의 성장과 함께 이차전지의 음극금속에 들어가는 동박의 수요가 크게 늘어나고 있다. 두께 10 µm 이하의 얇은 구리박인 동박은 이차전지 음극 집전체다. 동박은 전기화학반응에 필요한 전자를 공급하거나 전기화학반응으로 발생된 전자를 모아주는 역할을 한다. 이에 비해 두께가 2~4 µm 안팎의 초극박은 첨단소재다. 초극박은 주로 반도체 패키지, 데이터 센터, 5세대 이동통신(5G), 우주항공 산업반도체 인쇄회로기판(PCB), 이차전지 소재 등 고부가가치의 특수용도로 쓰인다. 이차전지의 음극소재인 동박은 배터리에서 발생되는 열을 외부로 방출하고, 전자의 이동 통로이자, 전극의 형상을 유지하는 지지체의 역할을 한다. 특히 이차전지의 용량 증가를 위해서는 단위 면적당 에너지 밀도가 높아져야 하고, 이를 위해 동박의 무게는 낮춰야 하기에 두께를 더욱 얇게 만들어 단위 부피당 면적은 더 넓게해야 한다. 이와 동시에 동박의 연신율과 인장 강도를 높이고 전지의 충방전 시 발생하는 열을 빠르게 해소해서 전지 수명을 늘일 수 있어야 한다. 동박은 이차전지 소재 중 초기설비 투자비가 가장 높아 신규 진입이 어렵다는 단점이 있으나, 다른 소재(코발트, 니켈, 망간 등) 대비 낮은 가격과 변동성이 적고 다른 산업 분야로의 확장성이 높아 소재로서의 많은 강점을 가지고 있다[1].
고객이 요구하는 다양한 물성의 동박을 제조하기 위하여 전해도금법을 주로 이용하지만 기본욕을 변경해가며 동박을 생산하기에는 유지비용과 폐액처리에 의한 환경적 문제 등의 어려움이 있다. 이로 인하여 일반적으로 전류밀도, 전류파형, 전극 간격, 첨가제, 유속, 음극 전압, 온도, 교반조건 등의 다양한 공정변수를 조절하여 원하는 특성을 갖는 제품을 생산하고 있다. 특히 미량 첨가되는 첨가제의 미세 조절은 동박의 표면 거칠기 및 기계적, 전기적 특성 제어를 가능하게 한다 [2-8]. 황산-황산구리 용액에 염화이온을 첨가한 기본액에 억제제(inhibiter), 평활제(leveler), 광택제(brightener) 등을 복합적으로 첨가하여 연속생산공정의 전해액으로 사용되고 있다[3, 9]. 대표적인 광택제로는 MPSA, SPS, DPS, Thiourea 등의 화합물이 사용되고[10-12], 억제제로는 콜라겐, PEG, PPG, 탄산칼륨(potassium carbonate) 등이 사용된다[13, 14]. 평활제는 PEI, JGB, HEC, PVP 등 화합물이 주로 사용 된다[15, 16]. 일반적으로 동박의 생산비 감축과 생산량 증대를 위하여 고전류 밀도로 생산이 가능한 첨가제 발굴이 필요하며, 전해액 내에서 첨가제의 역할과 이로 인한 동박의 표면특성 및 전기적 특성에 대한 연구가 필요하다. 또한 고객이 요구하는 다양한 특성을 만족하는 맞춤형 제품을 생산하기 위한 각각의 특성을 만족시키는 여러 종류의 첨가제 개발과 첨가제-물성의 상관관계에 대한 추가적인 연구가 절실히 필요하다. 전해도금 공정에 적용하기 위한 첨가제에 대한 연구 결과를 살펴보면 Kim 등[13, 17]은 싸이오요소와 젤라틴은 구리 박막의 부식 방지 및 표면 거칠기를 낮추는 효과가 있다 하였다. Kim 등[9, 18]은 평활제인 JGB 첨가제는 구리이온보다 전착층 돌출부에 먼저 흡착하여 돌출부에서의 구리이온의 전착을 방해함과 동시에, 구리이온이 함몰부로 이동하여 전착되도록 유도하여 평탄한 구리 도금층이 형성되게 한다. 또한 JGB 첨가시 전착층의 결정립의 크기가 감소하고 첨가량에 따라 억제 효과가 다르며, 전류 밀도가 일정량 이상 증가한 경우 평활제 효과가 감소한다 하였다[19-22]. 또한 Bonou [23] 등은 첨가제로 PEG와 염화이온을 복합적으로 적용하면 구리의 환원반응을 억제하는 효과와 억제효과 유지시간이 증가된다고 하였다. 그러나 PEG 단독으로 첨가하면 그 효과가 감소한다 하였다. 이러한 대부분의 연구결과들은 20 ASD 이상의 실제 조업 조건보다 낮은 10 ASD 이하의 전류밀도에서 연구한 결과이다. 또한 연속공정에서 음극으로 사용되고 있는 타이타늄 기지가 아닌 스퍼터링 공법으로 증착한 금(Au) 또는 구리(Cu) 박막을 이용하였다[3, 13, 17, 24]. 이처럼 일부 첨가제들이 연구되고 있지만 산업현장에서 조업에 활용하고 있는 고전류밀도(20 ASD이상)에서 동박의 특성을 향상 또는 제어할 수 있는 첨가제에 대한 연구는 부족한 사항이다.
이에 본 연구에서는 고전류밀도에서 탄산칼륨 첨가제를 개별적으로 첨가하였을 때 첨가량에 따른 초기 분극현상에 대한 연구를 실시한 후, 광택제, 평활제를 복합적으로 첨가하여 전착층의 표면 특성과 물성변화에 대한 상호 연관성에 대한 연구를 진행하였다.
2. 실험 방법
전해동박 제조를 위하여 기본욕으로 황산-황산구리(Cu: 50 g/L, H2SO4: 100 g/L) 수용액을 사용하였으며, 사각 전해조에 2 L의 전해액, 버블, 전극 그리고 첨가제를 첨가하여 실험을 진행하였다. 첨가제 중 억제제로는 탄산칼륨(potassium carbonate)를 평탄제는 Janus Green B(JGB)를 그리고 광택제는 3-mercapto-1-propane sulfonic acid (MPSA)를 사용하였다. 탄산칼륨 첨가제의 단독 첨가 및 첨가량의 변화에 따른 특성평가를 우선적으로 실시하였다. 불용성 양극으로는 타이타늄 위에 IrO2을 코팅한 전극을 사용하였으며, 음극으로는 순수 타이타늄 판을 #1500까지 순차적으로 연마하여 사용하였다. 또한 도금욕의 원활한 순환을 위하여 음극 기지로부터 50 mm 떨어진 곳에 버블을 공급하였다. 탄산칼륨 첨가제의 단독 첨가 및 첨가량에 따른 분극전압 측정을 위해서는 타이타늄을 1 cm2 의 크기로 제작하여 사용하였으며, 기계적 특성에 미치는 영향 평가를 위해서는 50 mm × 150 mm 크기의 타이타늄 기판을 사용하여 동박을 제조하였다. 음극과 양극의 거리는 10 cm 로 유지하였고, 도금액 온도는 50 °C(±0.5 °C)로 일정하게 유지하였다. 또한 도금욕의 원활한 순환을 위하여 버블을 이용하여 흐름을 형성하여 주었다. 전해도금은 전위차계(VersaSTAT3, AMETEK, U.S.A.)를 이용하여 정전류 모드에서 20 ASD로 진행하였으며, 전기적·기계적 물성분석을 위하여 도금층의 두께는 12 µm 되도록 하였다. 도금층 두께는 XRF(P type, BOWMAN, U.S.A.)장치를 통하여 확인하였다. 도금층의 표면형상 관찰을 위하여 주사전자현미경(FESEM, SU-70, Hitachi, Japan)을 활용하였으며 결정립 크기를 분석하기 위하여 X선 회절분석기(D8 ADVANCE, Bruker, Germany)를 사용하였다. 비저항을 측정을 위하여 4극 탐침법(CMT-SR1000N, AIT, Korea)장치를 사용하였고, 도금층 표면조도 측정은 표면조도측정기(SJ-400, Mitutoyo, Japan)를 활용하여 측정하였다. 도금층의 표면조도, 비저항, 인장강도 등 측정은 각각의 조건에서 6회 측정하였으며 통계 처리를 위하여 Minitab 프로그램을 사용하여 측정 결과를 분석하였다.
3. 결과 및 고찰
전해도금이 진행되는 동안 억제제인 탄산칼륨(potassium carbonate) 첨가제에 대한 효과를 확인하기 위하여 기본욕인 황산-황산구리 전해액에 탄산칼륨의 첨가량을 달리하여 진행하였으며, 조건은 표 1과 같다.
그림 1은 탄산칼륨 첨가제의 농도를 달리하여 전해도금을 진행하였으며, 도금 초기 0.2초 동안의 전압의 변화를 나타낸 결과이다. 황산-황산구리 기본욕(A) 조건 대비 탄산칼륨 첨가제를 5~30 ppm 첨가한(B~F) 경우의 초기 전압이 낮게 나타났으며, 첨가량이 40 ppm인(G) 경우에는 전압이 높게 나타났다. 5~10 ppm 첨가시 가장 낮은 전압을 20~25 ppm 범위 이상 첨가한 경우 전압이 상승하여 40 ppm 첨가한 조건에서는 무첨가 조건(A) 보다 높은 전압을 보이고 있다. 이러한 전압의 변화가 초기 표면에서의 구리 이온의 석출과의 관계를 확인하기 위하여 도금 표면을 관찰한 결과를 그림 2에 나타내었다.
Potential performance of the electrolyte at potassium carbonate additive with different concentrations.

SEM images of titanium surface tilted by 30°. Coppers were plated for 0.2 seconds at the addition of various potassium carbonate concentrations.
무첨가 조건(A) 대비 탄산칼륨을 5~10 ppm 첨가한 군(B, C)에서는 구리결정 형성이 적게 되었으며, 20~25 ppm 첨가한(D, E) 조건에서는 표면에 결정들이 확산되어 형성이 되었다. 그러나 첨가량이 30 ppm 이상인 경우(F, G)에는 결정들이 서로 응집하여 2 µm 이상의 큰 결정들로 성장하였다. 탄산칼륨 첨가제가 구리 이온이 타이타늄 표면에 흡착되는 것을 방해하여 기지 표면에 고르게 흡착되지 못하고 표면에너지가 적은 구리 결정에 흡착이 되면서 결정이 증대되는 것으로 보여진다. 적절한 첨가량을 첨가한 경우에 넓은 영역의 기지 표면에서 구리의 형성을 촉진하나 첨가량이 지나치게 많은 경우에는 기지에서의 구리 형성 보다는 기존에 형성된 결정에 흡착하여 결정이 성장하게 하는 역할을 하는 것을 확인할 수 있었다.
탄산칼륨 첨가제와 광택제, 평활제와의 상호관계를 확인하기 위하여 염화이온와 광택제 MPSA는 20 ppm으로 고정하였고, 평활제 JGB는 5 ppm, 10 ppm을 선정하였다. 표 2는 복합첨가제의 조건을 나타낸 것이다.
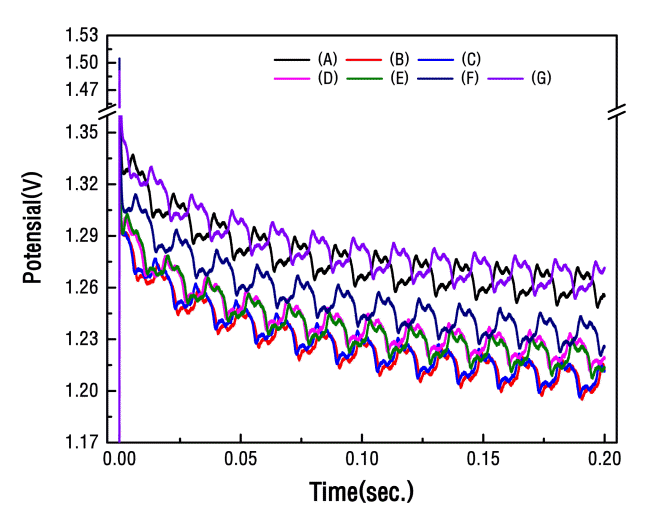
그림 3은 무첨가(a) 조건과 기본욕에 염화이온 20 ppm과 MPSA 20 ppm을 첨가한 조건(b)과 여기에 JGB 첨가제를 5~10 ppm 첨가한 조건(c, d) 그리고 탄산칼륨 첨가제의 농도를 달리하여 복합적으로 첨가한 조건(e~g)에 대한 초기 0.2초 동안의 전압을 나타낸 결과이다. 무첨가 조건대비 첨가제를 첨가한 모든 조건에서 높은 전압을 보이고 있다. 첨가제을 첨가한 (b)~(g) 조건에서 살펴보면, 염화이온 20 ppm과 MPSA 20 ppm을 첨가한 조건(b)에서 가장 낮은 전압을 보이고 있으며, 여기에 JGB를 5, 10 ppm 첨가한 경우 전압이 상승되었다. 이러한 현상은 JGB를 10 ppm 첨가한 경우 5 ppm을 첨가한 조건보다 더 증가되었다. 또한 JGB를 10 ppm 첨가하여 12 µm두께로 구리층을 도금하여 타이타늄 기지로부터 분리할 경우 분리가 원활하게 이루어지지 않고 구리층이 쉽게 찢어지는 현상이 발생하였다. 염화이온, MPSA, JGB 복합첨가시 JGB의 첨가량은 5 ppm으로 고정하고 탄산칼륨 첨가제를 10~30 ppm을 첨가하였다. 탄산칼륨 첨가제를 단독 첨가한 결과(그림 1)에서는 탄산칼륨 첨가량을 5~10 ppm 첨가시 가장 낮은 전압을 보였으나, 복합 첨가시에는 10 ppm(e)을 첨가한 조건보다 20 ppm(f) 첨가한 경우에 더 낮은 전압을 보이고 있다. 탄산칼륨 첨가량이 30 ppm(g) 조건의 경우 다시 전압이 증가하는 현상을 보이고 있다. 단독 첨가한 경우보다 복합 첨가한 경우에는 탄산칼륨의 첨가량이 증가되어야 전압을 낮추는 현상이 더 잘 나타나고 있다.

Potential performance of copper were plated for 0.2 seconds at various addition concentrations of the potassium carbonate additive.
그림 4는 0.2초간 도금된 표면을 관찰한 결과이다. 염화이온 20 ppm과 MPSA 20 ppm을 첨가한 조건(b)에서 일부 표면에서 별모양의 결정과 반구형태 등 다양한 형태의 결정이 형성되었고 JGB를 5 ppm을 추가적으로 첨가된(c) 경우에는 결정들이 군집되는 현상과 10 ppm첨가한(d) 경우에는 결정들이 별모양으로 뾰족한 형상을 보이고 있다. 또한 탄산칼륨을 10~30 ppm을 복합적으로 첨가한(e~g) 조건에서는 10 ppm 첨가한(e) 조건에서는 3가지 첨가제를 첨가한(c) 조건대비 결정이 군집되는 현상은 감소하였으나, 탄산칼륨의 첨가량이 증가되면서 군집되는 현상과 별모양의 결정이 발생되고 있다. 첨가제간의 상호작용과 구리이온과의 반응 그리고 기지 표면에서의 전착반응 등 다양한 반응이 복합적으로 작용되고 있어 명확한 군집현상의 원인을 규명하기에는 어려움이 있다.

FESEM images of titanium surface tilted by 30°. Coppers were electroplated for 0.2 seconds at the addition of various additives concentrations.
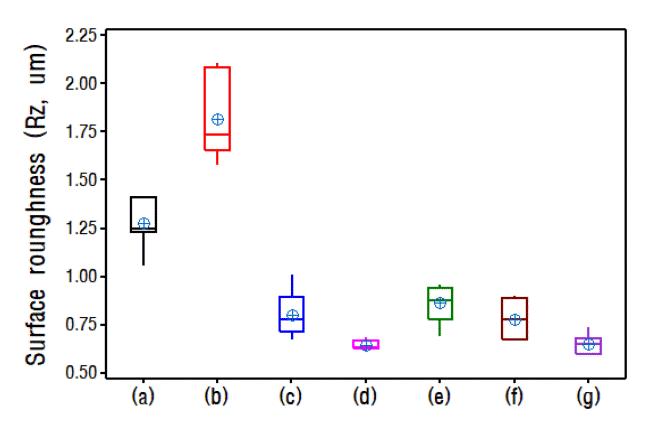
그림 5는 12 µm두께로 구리 전착층을 도금한 표면을 관찰한 이미지이다. 무첨가한 대비 염화이온 20 ppm과 MPSA 20 ppm을 첨가한 조건(b)을 제외하고는 표면이 치밀한 조직을 보이고 있다. 염화이온 20 ppm과 MPSA 20 ppm을 첨가한 조건(b)의 경우 표면에 각기둥 모양의 결정들이 표면에 존재하였다. 광택제, 억제제, 평활제 및 염화이온을 복합적으로 첨가한 조건(e~g)에서 표면에 원형의 큰 결정들이 존재하는 것으로 보여지나 단차를 확인한 그림 6의 결과를 보면, 결정과 표면간의 단차는 1 µm 이하이다. 표면조도 결과 그림 6에서 보면 염화이온 20 ppm과 MPSA 20 ppm을 첨가한 조건(b)을 제외하고는 무첨가(a) 조건 대비 표면 조도(Rz)가 낮게 나타나고 있다. 또한 탄산칼륨 첨가제를 10~30 ppm 복합적으로 첨가한 조건의 표면조도는 첨가량이 증가할수록 평균값은 감소하였으나, 통계적으로 유의차는 없었다(p-value: 0.001).

FESEM images(low magnification) of copper foil tilted by 30°. Copper foils were plated for 12 µm at the addition of various additives concentrations.
그림 7은 도금층에 대한 비저항을 측정한 결과이다. 비저항의 경우 염화이온과 MPSA 각각 20 ppm에 JGB 10 ppm을 첨가한(d) 조건을 제외하고 무첨가(a) 조건보다 높은 비저항을 나타내고 있다. (d) 조건에서 비저항이 낮고 비저항의 편차가 크게 나타나고 있는 이유로는 초기 결정의 형성 및 성장이 별모양의 각형구조의 결정 성장이 이루어져 결정의 성장방위 및 표면조도 등 복합적인 영향이 있을 것으로 생각되며 뒤에서 다시 다루도록 하겠다.
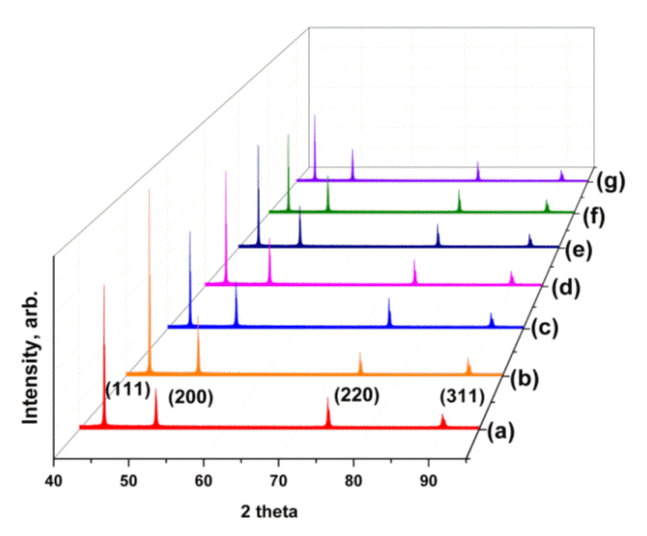
도금층의 결정구조를 확인하기 위하여 XRD 분석한 결과를 그림 8에 나타내었다. 측정결과 모든 실험 조건에서(111) 방위의 피크가 가장 강하게 나타났으며 피크의 강도 또한 비슷한 양상을 보이고 있다. 그림 9는 Yoshimura [25] 등이 제안한 orientation index(M) 분석법을 이용하여 결정성장 방위를 분석한 결과를 나타낸 것이다. (220)면을 갖는 시편의 경우 아래와 같은 방법으로 orientation index(M)를 계산하였다.
IFR(220)=IF(220)/{IF(111)+IF(200)+IF(220)+IF(311)}
IR(220)=I(220)/{I(111)+I(200)+I(220)+I(311)}
M(220)=IR(220)/IFR(220)
위에서 IF(220)은 XRD 강도의 이론값이며 I(220)은 실험을 통해 측정된 값이다. 만약 분석된 M값이 1보다 큰 수를 가진다면 이는 도금층이 (220)면에 평행한 방위로 우선성장을 한다는 것이고, M값이 1보다 작은 경우 그 방위로의 우선성장이 둔화 되었다는 것을 의미한다.
염화이온 20 ppm과 MPSA 20 ppm을 첨가한 조건(b)을 제외하고는 우선성장방위로는 모든 조건에서 (220)에 평행하게 결정들이 성장하고 있음을 확인 할 수 있으며, (220) 방위로의 우선성장의 상대적 강도에는 차이를 보이고 있다. 염화이온 20 ppm과 MPSA 20 ppm을 첨가한 조건(b)은 (111) 방위로 우선성장을 하고 있으며, 무첨가(a) 조건의 경우에는 (220), (111) 방위로 우선성장을 하고 있다. JGB를 5 ppm 복합적으로 첨가한 경우(c) (220) 방위로의 우선성장이 증가되었고, 탄산칼륨을 추가적으로 첨가시키는 경우 (220) 방위로의 우선성장은 탄산칼륨 무첨가 조건(c) 대비 감소되었다.
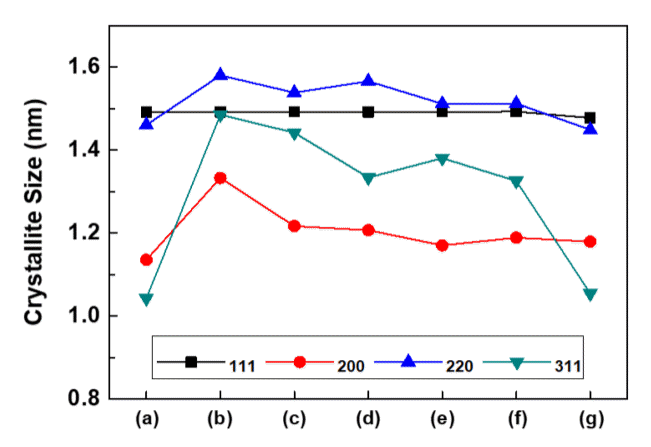
그림 10은 XRD 분석 결과를 이용하여 결정의 크기를 구하기 위하여 Scherrer식(1)을 활용하여 분석한 결과이다[26, 27]. 식 (1)에서 λ는 타겟 파장(Cu: 0.154056 nm), B는 시편에서 측정된 반가폭, θ는 회절각 2θ의 절반 값이다.
그림 9에서 우선성장방위로 나타난 (220), (111)방위의 결정립 크기를 살펴보면, (111)방위의 경우 결정립 크기의 변화가 관찰되지 않았으며, (220) 방위의 경우 염화이온 20 ppm과 MPSA 20 ppm을 첨가한 조건(b)에서 가장 큰 결정립 크기를 나타내고 있으며, JGB 5 ppm 첨가시 결정립이 감소하고 여기에 탄산칼륨 첨가제를 첨가한(e~g) 경우 결정립의 크기는 더욱더 감소하였다. 이러한 경향은 (311) 방위에서 더욱 뚜렷하게 나타나고 있다. 이를 통하여 억제제인 탄산칼륨 첨가제에 의한 결정립 크기의 감소효과를 확인 할 수 있었다.
그림 11은 구리 전착층의 인장 시험의 대표적인 결과를 응력-변형률 그래프로 나타낸 것이다. 구리 전착시 첨가제의 종류와 첨가량에 따라 기계적 성질이 달라지는 것을 볼 수 있다. 염화이온 20 ppm과 MPSA 20 ppm 그리고 JGB를 10 ppm 첨가한 조건(d)의 경우 인장시험을 위한 시편 제작 시 쉽게 부서져 측정이 불가능하였다. 무첨가 조건(a) 대비 모든 조건에서 최대인장강도는 낮게 나타나고 있으며, 염화이온 20 ppm과 MPSA 20 ppm을 첨가한 조건(b)은 탄성영역 이후 소성영역이 길게 나타나고 있다. 또한 JGB, 탄산칼륨을 첨가한 (c)~(g) 조건에서 소성영역이 매우 짧게 나타남을 확인할 수 있었다. 좀 더 자세한 인장강도 및 연신율을 분석한 결과를 그림 12에 나타내었다. 그림 11에서도 확인 하였듯이 무첨가(a) 대비 염화이온 20 ppm과 MPSA 20 ppm 조건(b)에서 인장강도는 감소하였고, 연신율은 증가하였다. 이는 Hall-Petch 효과에 의해 결정립의 크기가 증가하면 인장 강도가 감소해야 한다는 이론과 잘 부합한다. 그러나 탄산칼륨을 30 ppm 첨가한(g) 조건을 제외한 경우 무첨가 조건 대비 결정립의 크기가 증가하고 인장강도가 감소하였으나 연신율은 증가하지 않고 오히려 감소하였다. 또한 탄산칼륨 첨가량에 따른 인장강도 및 연신율은 유의차가 없었다(p-value: 0.000).
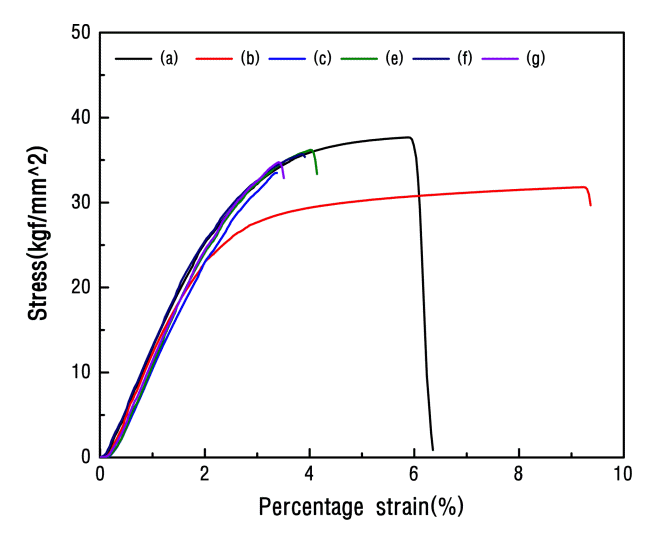
Representative stress-strain curves of pure copper layer and various additives concentration copper layers.
4. 결 론
산업적으로 중요성이 높아지고 있는 전해동박의 물성 향상을 위한 노력이 절실히 필요한 시기이다. 전해동박 생산은 연속도금공정으로 고전류밀도 조건에서 이루어지고 있다. 따라서 고전류밀도에서의 첨가제 적용가능성과 첨가제에 의한 표면특성 및 전기적 특성, 구조적 특성 변화에 대하여 연구하였다. 억제제인 탄산칼륨(potassium carbonate)의 단독 첨가와 기본적으로 평활제, 광택제를 첨가하고 탄산칼륨 첨가제의 양을 변화시켜 복합적으로 첨가한 후 도금층의 변화에 대하여 연구를 진행하였다.
1. 탄산칼륨 첨가제를 단독으로 첨가한 경우에는 5~25 ppm 첨가시 초기의 도금 전압을 낮추는 효과를 확인할 수 있었으며, 초기 결정들이 응집하지 않고 표면에 고르게 분포하기 위해서는 20~25 ppm 범위내에서 첨가가 타당하다. 그러나 실제 전해동박 생산이 이루어지는 현장에서는 첨가제를 복합적으로 사용하고 있다.
2. 첨가제를 복합적으로 첨가한 경우 전착층의 경우 탄산칼륨 첨가량에 의한 표면 조도 및 비저항의 변화는 유의 차가 없었으나, (220) 방위로의 우선성장 상대적 강도는 10 ppm 대비 20 ppm에서 증가하였다.
3. 복합 첨가 조건에서 탄산칼륨 첨가량이 증가할수록 결정립의 크기가 감소하였으나, 인장강도 및 연신율의 변화는 미비하였다(p-value: 0.000). 첨가제 JGB의 첨가량이 10 ppm의 경우 타이타늄 기지와의 분리 및 기계적 물성 분석이 어려울 정도로 물성이 불안정하기에 첨가량 선정에 주의가 필요하다. 또한 균일한 물성을 확보하기 위해서는 탄산칼륨의 첨가량은 10~20 ppm 범위에서 첨가하는 것이 타당하리라 생각된다.