1. ņä£ ļĪĀ
ņ×ÉņÖĖņäĀ ņ░©ļŗ©ņåīņ×¼ļŖö ņØ╝ļ░śņĀüņ£╝ļĪ£ ņ×ÉņÖĖņäĀņØä ĒØĪņłśĒĢśņŚ¼ ņŚÉļäłņ¦Ć ļ│ĆĒÖśņØä ņ£ĀļÅäĒĢśļŖö ņ£ĀĻĖ░Ļ│äņØĖ ĒśĖļ¬©ņé┤ļĀłņØ┤ļō£, ņśźĒŗĖņé┤ļ”¼ņŗżļĀłņØ┤ĒŖĖ ļō▒ņØ┤ ņ׳Ļ│Ā, ņ×ÉņÖĖņäĀņØä ņé░ļ×Ć, ĒØĪņłśĒĢśļŖö ļ¼┤ĻĖ░Ļ│äņØĖ TiO2ņÖĆ ZnOĻ░Ć ļäÉļ”¼ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŗż. ĻĘĖ ņżæ ZnOļŖö ļ¼┤ĻĖ░Ļ│ä ņ×ÉņÖĖņäĀ ĒØĪņłśņĀ£ ņżæņŚÉņä£ļÅä Ēł¼ļ¬ģņä▒ņØ┤ ļåÆĻ│Ā ņ░©ļŗ©ņśüņŚŁņØ┤ ļäōņ¢┤ ņ×ÉņÖĖņäĀ ņ░©ļŗ©ņĀ£ļĪ£ ļ¦ÄņØ┤ ņō░ņØ┤Ļ│Ā ņ׳ļŗż [1-3]. ĒĢśņ¦Ćļ¦ī ņ×ÉņÖĖņäĀ ņ░©ļŗ©ņĀ£ļŖö ļĢĆĻ│╝ Ēö╝ņ¦ĆņŚÉ ņØśĒĢ┤ ņēĮĻ▓ī ņ¦Ćņøīņ¦ĆļŖö ļ¼ĖņĀ£Ļ░Ć ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ Ēö╝ņ¦ĆĻ▓ĮĒÖö ĒŖ╣ņä▒ņØä Ļ░¢ļŖö ZnOĻ░Ć ĒĢäņÜöĒĢśļŗż. ĒĢ┤ņä£ ļ│Ė ņŚ░ĻĄ¼ļŖö ņ×ÉņÖĖņäĀ ņ░©ļŗ©ņĀ£ņØś ņÜ®ļÅäļĪ£ ņé¼ņÜ®ĒĢśĻĖ░ ņÜ®ņØ┤ĒĢśĻ│Ā Ēö╝ņ¦ĆĻ▓ĮĒÖö ĒŖ╣ņä▒ņØä Ļ░¢ļŖö ZnO powderņØś ĒĢ®ņä▒ņŚÉ ļīĆĒĢśņŚ¼ ņŚ░ĻĄ¼ĒĢśņśĆļŗż. ņØ┤ņÖĆ Ļ░ÖņØ┤ ļ¦īļōżņ¢┤ņ¦ä ZnO powderļŖö ņé¼ļ×īņØś Ēö╝ņ¦Ćņä▒ļČäņŚÉ ļīĆĒĢśņŚ¼ Ļ│ĀĒØĪņ£Ā ĒŖ╣ņä▒ņØä Ļ░¢Ļ│Ā ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ņé¼ļ×īņØś Ēö╝ļČĆņÖĆ ļ¦ÄņØ┤ ņĀæņ┤ēļÉśļŖö ņ×ÉņÖĖņäĀ ņ░©ļŗ©ņĀ£ Ēś╣ņØĆ Ē¢źĻĘĀ ĒĢäļ”ä ļō▒ņŚÉ ņ£ĀņÜ®ĒĢśĻ▓ī ņō░ņØ╝ ņłś ņ׳ļŗż. ZnO powderļź╝ ĒĢ®ņä▒ĒĢśĻĖ░ ņ£äĒĢśņŚ¼ ZnO ĒĢ®ņä▒ņŚÉ ņŻ╝ļĪ£ ņō░ņØ┤ļŖö ZnCl2Ļ│╝ NaOHņØä ņé¼ņÜ®ĒĢśņśĆĻ│Ā, Ļ│ĄņĀĢļ░®ņŗØņØĆ ņłśņŚ┤ĒĢ®ņä▒ļ▓ĢņØä ņé¼ņÜ®ĒĢśņŚ¼ ņŚ░ĻĄ¼ļź╝ ņ¦äĒ¢ēĒĢśņśĆļŗż [4-6]. ņĀ£ņĪ░Ļ│ĄņĀĢ ņĪ░Ļ▒┤ņØś ļ│ĆņłśļĪ£ļŖö ļ░śņØæņś©ļÅäņÖĆ NaOHņØś ļ╣äņ£© ĻĘĖļ”¼Ļ│Ā ĒĢ®ņä▒ņŗ£ņØś ņś©ļÅäļź╝ ļ│ĆņłśļĪ£ ļæÉĻ│Ā ņŚ░ĻĄ¼ļź╝ ņ¦äĒ¢ēĒĢśņśĆļŗż [7]. ņŗżĒŚśņØś Ļ│ĄņĀĢ ņ¦äĒ¢ēņØĆ ZnCl2Ļ│╝ NaOHļź╝ ņäżņĀĢņĪ░Ļ▒┤ņØś ļ╣äņ£©ļīĆļĪ£ ļ¦īļōĀ ņÜ®ņĢĪņØä pHļåŹļÅäļź╝ ņĪ░ņĀłĒĢ£ ņÜ®ņĢĪņŚÉ ļÅÖņŗ£ņŚÉ droppingĒĢ£ Ēøä ņĪ░Ļ▒┤ņŚÉ ļö░ļźĖ ņś©ļÅäņŚÉņä£ ļ░śņØæņØä ņŗ£Ēé©ļŗż. ļ░śņØæņØ┤ ņÖäļŻīļÉ£ ņĪĖ ņāüĒā£ņØś ZnOļź╝ ņŚ¼Ļ│╝ĒĢśņŚ¼ 100 ┬░CņŚÉņä£ Ļ▒┤ņĪ░ļź╝ ņŗ£ņ╝£ powderĒśĢĒā£ļĪ£ ņĀ£ņĪ░ĒĢśņśĆļŗż. X-Ray Diffraction (SmartLab Rigaku 9 kW)ņØä ņé¼ņÜ®ĒĢśņŚ¼ ZnOņØś Ļ▓░ņĀĢņä▒ņØä ĒÖĢņØĖĒĢśņśĆĻ│Ā, Scanning Electron Microscope (Nova NanoSEM 450)ļĪ£ ņ×ģņ×ÉņØś Ēü¼ĻĖ░ņÖĆ ĒśĢĒā£ļź╝ Ļ┤Ćņ░░ĒĢśņŚ¼ ņĀ£ņĪ░Ļ│ĄņĀĢņŚÉ ļö░ļźĖ ņ×ģņ×ÉĒü¼ĻĖ░ņÖĆ ĒśĢĒā£ņØś Ļ▓ĮĒ¢źņä▒ņØä ļČäņäØĒĢśņśĆļŗż. gelling testļŖö ļÅÖņŗØļ¼╝ ņ¦Ćļ░®ņé░ņØś ņŻ╝ņøÉņåīņØĖ oleic acidļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ powderņØś Ēö╝ņ¦ĆĻ▓ĮĒÖö ņåŹļÅäļź╝ Ļ┤Ćņ░░ĒĢśņśĆļŗż.
2. ņŗżĒŚśļ░®ļ▓Ģ
2.1 ZnO powderņØśņĀ£ņĪ░
ĻĘĖļ”╝ 1ņØĆ ņłśņŚ┤ĒĢ®ņä▒ļ▓ĢņØä ņĀüņÜ®ĒĢ£ ZnO powder ņĀ£ņĪ░ļź╝ ņ£äĒĢ£ Ļ│╝ņĀĢņØä ļ¬©ņŗØļÅäļĪ£ ļéśĒāĆļéĖ Ļ▓āņØ┤ļŗż.
PowderņØś ņĀ£ņĪ░ļ░®ļ▓ĢņØĆ ņłśņŚ┤ĒĢ®ņä▒ļ▓Ģņ£╝ļĪ£, ņ▓©Ļ░Ć ņłśņÜ®ņĢĪņØĆ ZnCl2ņÖĆ NaOHļź╝ ņĀäĻĄ¼ņ▓┤ļĪ£ ņé¼ņÜ®ĒĢśĻ│Ā, ņŗ£ņ×æņÜ®ņĢĪņØĆ NaOHņłśņÜ®ņĢĪņØä ņØ┤ņÜ®ĒĢśņŚ¼ pH 13ņØś ņŚ╝ĻĖ░ņä▒ ļČäņ£äĻĖ░ļź╝ ņ£ĀļÅäĒĢśņśĆļŗż.
ZnCl2ņÜ®ņĢĪņØś ņé░ĒÖöļ░śņØæņØä ņ£ĀļÅäĒĢśĻĖ░ ņ£äĒĢ┤ ņŗ£ņ×æņÜ®ņĢĪņŚÉ NaOH ņÜ®ņĢĪņØä Ļ░ÖņØ┤ ļäŻĻ│Ā 1ņ░© ļ░śņØæņØä ņŗ£ņ╝░ļŗż. ņÜ®ņĢĪņØś dropping ņåŹļÅäļŖö 1hņ£╝ļĪ£ ļüØļéśļÅäļĪØ Ē¢łĻ│Ā stirring ņåŹļÅäļŖö 200 RPMņ£╝ļĪ£ ĻĄÉļ░śņØä ĒĢśņśĆļŗż.
1ņ░© ļ░śņØæņØ┤ ļüØļé£ ĒøäņŚÉ Ļ│Āņś©ņØś ņś©ļÅäņŚÉņä£ 4hļÅÖņĢł 2ņ░© ļ░śņØæņ£╝ļĪ£ ņłÖņä▒ņØä ņ¦äĒ¢ēĒĢśņśĆļŗż [8]. ņĄ£ņóģņĀüņ£╝ļĪ£ ņŚ¼Ļ│╝ļź╝ ĒåĄĒĢ┤ ņłśļČäĻ│╝ ļČäņł£ļ¼╝ņØä ņĀ£Ļ▒░ĒĢ£ Ēøä 100 ┬░CņŚÉņä£ Ļ▒┤ņĪ░ĒĢśņŚ¼ powderļź╝ ņĀ£ņĪ░ĒĢśņśĆļŗż.
ZnO powderņØś ņĀ£ņĪ░ļź╝ ņ£äĒĢ£ Ļ│ĄņĀĢ ņŗ£ņŖżĒģ£ņ£╝ļĪ£ļŖö, ņłśņÜ®ņĢĪņØä droppingĒĢśļŖö Metering pump (Jenie Wellņé¼ JWSE-100)ļŖö ļæÉ Ļ░£ļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ļÅÖņŗ£ņŚÉ droppingņØ┤ ļüØļéśļÅäļĪØ ĒĢśņśĆĻ│Ā, ņłśņÜ®ņĢĪņØ┤ ļōżņ¢┤ņ׳ļŖö ņÜ®ņĢĪņØĆ droppingĒĢśļŖö ļÅÖņĢł Agitator (IKAņé¼ EUROSTAR 20)ņØä ņé¼ņÜ®ĒĢśņŚ¼ 200 RPMņ£╝ļĪ£ ĻĄÉļ░śņØä ĒĢśņśĆļŗż. DroppingņØ┤ ļüØļé£ Ēøä heating mantle (MTOPSņé¼ MSDMB)ņØä ņé¼ņÜ®ĒĢśņŚ¼ Ļ│Āņś©ņŚÉņä£ ļ░śņØæĒĢśņśĆļŗż.
Ēæ£ 1ņØĆ ņĪ░Ļ▒┤ļ│Ćņłśļź╝ ņĀĢļ”¼ĒĢ£ Ļ▓āņ£╝ļĪ£ ņĪ░Ļ▒┤ļ│ĆņłśļŖö 1ņ░©ļ░śņØæņŗ£ ņ▓©Ļ░Ć ņÜ®ņĢĪņØĖ NaOHņłśņÜ®ņĢĪņŚÉ ļōżņ¢┤Ļ░ĆļŖö NaOHņ¢æĻ│╝ 2ņ░©ļ░śņØæņŗ£ ņłÖņä▒ ņś©ļÅäļĪ£ ļæÉĻ│Ā ņ¦äĒ¢ēĒĢśņśĆļŗż. NaOHņØś ņĪ░Ļ▒┤ņØĆ ZnCl2ņÖĆ molņ¦łļ¤ē ĻĖ░ņżĆ 1:1ļ╣äņ£©ņØĖ 84 gņØä ĻĖ░ņżĆņ£╝ļĪ£ 5%ņö® ņżäņŚ¼ 80 g, 76 g, 72 gņ£╝ļĪ£ ņĀĢĒĢśņśĆļŗż.
Ēæ£ 2ļŖö ņś©ļÅäņĪ░Ļ▒┤ņ£╝ļĪ£ NaOHņ¢æņØ┤ 76 g, ņś©ļÅäĻ░Ć 60 ┬░CņØĖ ņāśĒöīņØä ĻĖ░ņżĆņ£╝ļĪ£ 20 ┬░Cņö® ņś¼ļ”░ 80 ┬░C, 100 ┬░C ĻĘĖļ”¼Ļ│Ā 20 ┬░C ļé┤ļ”░ 40 ┬░CļĪ£ ņĪ░Ļ▒┤ņØä ņĀĢĒĢśņśĆļŗż.
2.2 ZnO powderņØś ĒŖ╣ņä▒ĒÅēĻ░Ć
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ņé¼ņÜ®ļÉ£ ĒŖ╣ņä▒ĒÅēĻ░ĆļŖö gelling testņÖĆ XRD, SEMņØä ņé¼ņÜ®ĒĢśņśĆļŗż. gelling testņŚÉ ņé¼ņÜ®ļÉ£ ņŗ£ņĢĮņØĆ ņ¦Ćļ░®ņé░ ņä▒ļČäņØĖ oleic acidļź╝ ņé¼ņÜ®ĒĢśņśĆĻ│Ā oleic acidļź╝ powderņÖĆ 10:1ļ╣äņ£©, 200 RPMņ£╝ļĪ£ ĻĄÉļ░śņØä ĒĢśņŚ¼ ļ░śņØæĒĢśņŚ¼ Ļ│Āņ▓┤Ļ░Ć ļÉśļŖö ņŗ£Ļ░äņØä ĒÖĢņØĖĒĢśņśĆļŗż. XRDļŖö ZnOņØś Ļ▓░ņĀĢņä▒ņØä ĒÖĢņØĖĒĢśĻĖ░ ņ£äĒĢ┤ ņĖĪņĀĢņØä ĒĢśņśĆĻ│Ā 2-ThetaļŖö 20ļČĆĒä░ 80Ļ╣īņ¦Ć, currentļŖö 200 mAļĪ£ ņĖĪņĀĢņØä ĒĢśņśĆļŗż. SEMņØĆ ZnOņØś ĒśĢĒā£ņÖĆ Ēü¼ĻĖ░ļź╝ ņĖĪņĀĢĒĢśĻĖ░ ņ£äĒĢ┤ Ļ┤Ćņ░░ĒĢśņśĆĻ│Ā 10 kVņŚÉņä£ ņĢĮ 100000ļ░░ļĪ£ ņĖĪņĀĢņØä ĒĢśņśĆļŗż.
3. Ļ▓░Ļ│╝ ļ░Å Ļ│Āņ░░
3.1 Zinc oxide powderņØś XRD ĒŖ╣ņä▒ĒÅēĻ░Ćļź╝ ĒåĄĒĢ£ Ļ▓░ņĀĢņä▒ ĒÖĢņØĖ
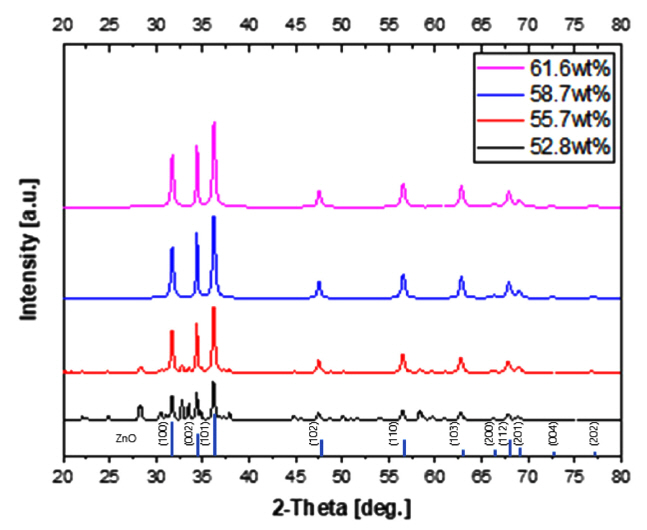
ĻĘĖļ”╝ 2ļŖö NaOHņØś ļåŹļÅä ļ╣äņ£©ņŚÉ ļö░ļźĖ ņāśĒöīļōżņØś XRD ĻĘĖļלĒöäļź╝ ļ╣äĻĄÉĒĢ£ ĻĘĖļלĒöäļĪ£ NaOHņØś ļåŹļÅäĻ░Ć 61.6 wt%, 58.7 wt%ļŖö ņł£ņłśĒĢ£ ZnOņØś peakņØ┤ ļéśĒāĆļé£ Ļ▓āņØä ĒÖĢņØĖ ĒĢĀ ņłś ņ׳ņŚłļŗż [9-10]. 55.7 wt%ņÖĆ 52.8 wt%ļŖö ZnO peakņØ┤ ļ░£Ļ▓¼ļÉśņŚłņ¦Ćļ¦ī ļŗżļźĖ Ļ▓░ņĀĢņØś peakņØ┤ ļéśĒāĆļé¼Ļ│Ā Simonkolleite Ļ▓░ņĀĢ peakņ£╝ļĪ£ ĒīÉļŗ©ļÉśņŚłļŗż [11-12].
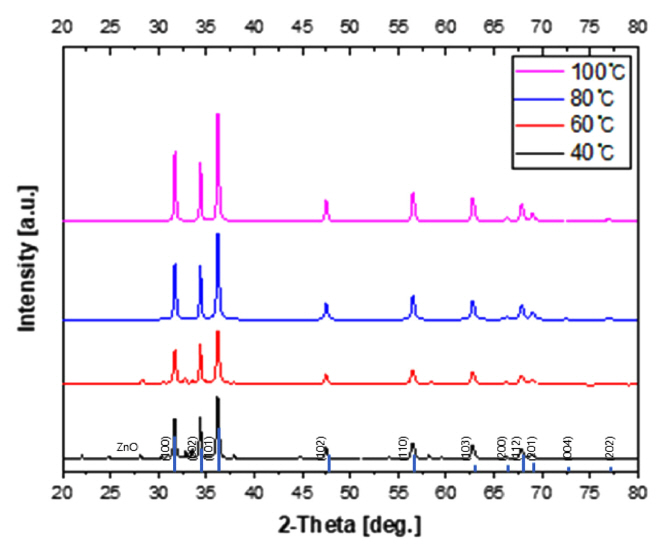
ĻĘĖļ”╝ 3ņŚÉņä£ļŖö 80 ┬░C, 100 ┬░CļŖö ZnO peakļ¦ī ĒÖĢņØĖļÉśņŚłņ¦Ćļ¦ī 40 ┬░CņÖĆ 60 ┬░CņŚÉņäĀ ZnOņÖĆ SimonkolleiteņØś peakņØ┤ Ļ░ÖņØ┤ ļéśņś© Ļ▓āņØä ĒÖĢņØĖ ĒĢĀ ņłś ņ׳ņŚłļŗż.
SimonkolleiteņÖĆ ZnO peakņØ┤ Ļ░ÖņØ┤ ļéśņś© ņāśĒöīņØĆ NaOH ļåŹļÅä 52.8 wt%, 55.7 wt% ĻĘĖļ”¼Ļ│Ā ļ░śņØæņś©ļÅä 40 ┬░C, 60 ┬░CņØĖ Ļ▓āņ£╝ļĪ£ ĒÖĢņØĖļÉśņŚłļŗż.
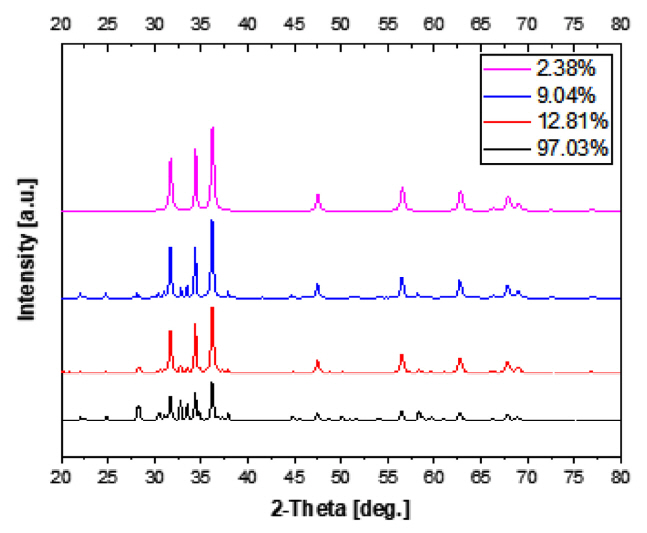
ĻĘĖļ”╝ 4ļŖö ZnOņÖĆ SimonkolleiteĻ░Ć Ēś╝ņ×¼ļÉ£ ņāśĒöīņØś ļ╣äņ£©ņŚÉ ļö░ļźĖ XRD ĻĘĖļלĒöäļź╝ ļ╣äĻĄÉĒĢ£ Ļ▓āņ£╝ļĪ£ Simonkolleite, ZnOņØś Ļ░üĻ░üņØś base peakņØä ĻĖ░ņżĆņ£╝ļĪ£ Simonkolleite/ZnOņØä ļ╣äņ£©ļĪ£ ņĀĢĒĢśņśĆļŗż. Ēś╝ņ×¼ļÉ£ ņāśĒöīņØś Simonkolleite/ZnOļ╣äņ£©ņØĆ 97.03%, 12.81%, 9.04% ņØ┤Ļ│Ā ZnO peakļ¦ī ĒÖĢņØĖļÉ£ ņāśĒöīņØĆ 2.38%ļĪ£ ļéśļ©Ėņ¦Ć ņāśĒöīĻ│╝ ļ╣äĻĄÉĒĢ┤ ļ│┤ņĢśņØä ļĢī ļŗżļźĖ ĒśĢĒā£ņØś peakĻ│╝ ļé«ņØĆ ļ╣äņ£©ļĪ£ ĒÖĢņØĖļÉśņŚłļŗż.
3.2 FE-SEMņØä ĒåĄĒĢ£ powderņØś Ēü¼ĻĖ░ ļ░Å ĒśĢņāü ĒŖ╣ņä▒ Ļ┤Ćņ░░
ĻĘĖļ”╝ 6ļŖö NaOHņØś ļåŹļÅä ļ╣äņ£©ņŚÉ ļö░ļźĖ ņāśĒöīņØś SEM Ļ▓░Ļ│╝ļź╝ ņĀĢļ”¼ĒĢ£ Ļ▓āņ£╝ļĪ£ powderņØś Ļ▓░ņĀĢ ĒśĢĒā£ņÖĆ Ēü¼ĻĖ░ļź╝ ļ╣äĻĄÉĒĢśņśĆļŗż. (a)ļŖö 800 nm ~ 1 ┬ĄmļĪ£ ļŗżļźĖ ņāśĒöīņŚÉ ļ╣äĒĢ┤ Ēü░ Ēü¼ĻĖ░ņØś ĒīÉņāüņØś ĒśĢņāüņ£╝ļĪ£ Ļ┤Ćņ░░ļÉśņŚłļŗż. (b)ņØś Ļ▓ĮņÜ░ ĒīÉņāüĻ│╝ ņ×æņØĆ ņ×ģņ×ÉĻ░Ć Ļ░ÖņØ┤ ļČäĒżļÉśļŖö ĒśĢņāüņØä ļ│┤ņśĆĻ│Ā (c), (d)ļŖö ņ×æņØĆ Ēü¼ĻĖ░ņØś ņ╣©ņāüĻ│╝ ĒīÉņāüņØ┤ Ēś╝ĒĢ®ļÉ£ ĒśĢņāüņ£╝ļĪ£ Ļ┤Ćņ░░ļÉśņŚłļŗż.
ĻĘĖļ”╝ 7ņØĆ ņś©ļÅä ļö░ļźĖ ņāśĒöīņØś SEM Ļ▓░Ļ│╝ļź╝ ņĀĢļ”¼ĒĢ£ Ļ▓āņ£╝ļĪ£ (a)Ļ░Ć Ēü░ Ēü¼ĻĖ░ņØś ĒīÉņāüĒśĢ ĻĘĖļ”¼Ļ│Ā (d)ļŖö ņ×æņØĆ Ēü¼ĻĖ░ņØś ņ£ĪĻ░üĒśĢ ĒśĢņāüņØ┤ Ļ┤Ćņ░░ ļÉśņŚłļŗż. (b), (c)ļŖö ņ×æņØĆ Ēü¼ĻĖ░ņØś ņ×ģņ×ÉņÖĆ ĒīÉņāüĒśĢņØ┤ Ēś╝ĒĢ®ļÉ£ ĒśĢņāüņØ┤ Ļ┤Ćņ░░ ļÉśņŚłļŗż.
NaOHņØś ļ╣äņ£©Ļ│╝ ĒĢ®ņä▒ ņś©ļÅäĻ░Ć ļé«ņØäņłśļĪØ ĒīÉņāü ĒśĢĒā£ņØś Ēü░ Ēü¼ĻĖ░Ļ░Ć ļéśĒāĆļéśĻ│Ā NaOHņØś ļ╣äņ£©Ļ│╝ ĒĢ®ņä▒ ņś©ļÅäĻ░Ć ļåÆņØäņłśļĪØ ņ×æņØĆ Ēü¼ĻĖ░Ļ░Ć ļéśĒāĆļéśļŖö Ļ▓āņØä ĒÖĢņØĖĒĢśņśĆĻ│Ā ĒīÉņāüņØ┤ ļéśĒāĆļéĀņłśļĪØ ņ¦¦ņØĆ gelling timeņØä Ļ░¢ļŖö Ļ▓āņØä Ļ│Āņ░░ĒĢśņśĆļŗż.
3.3 Oleic acid ņÜ®ņĢĪņØä ņé¼ņÜ®ĒĢ£ ZnO powderņØś gelling time test
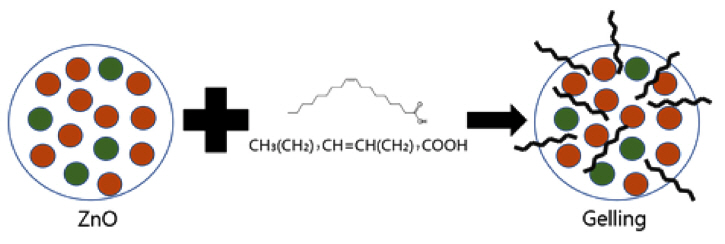
Gelling time testļŖö ļÅÖņŗØļ¼╝ņŚÉ ņĪ┤ņ×¼ĒĢśļŖö ņ¦Ćļ░®ņé░ ņä▒ļČäņØś oleic acidņŚÉ powderļź╝ 10:1ņØś ļ╣äņ£©ļĪ£ ĻĄÉļ░śĒĢśņŚ¼ Ļ│Āņ▓┤ĒÖö ĒĢśļŖö ņŗ£Ļ░äņØä ņĖĪņĀĢĒĢ£ ĒŖ╣ņä▒ĒÅēĻ░Ć ņØ┤ļŗż. GellingņŚÉ Ļ┤ĆĒĢ£ ņøÉļ”¼ļŖö ĻĘĖļ”╝ 8Ļ│╝ Ļ░ÖņØ┤ ZnOņØś ņ×ģņ×Éļōż ņé¼ņØ┤ļĪ£ oleic acidņØś ņłśņåīņÖĆ Ēāäņåī Ļ╝¼ļ”¼Ļ░Ć ļČÖņ¢┤ņä£ ļ░śņØæĒĢśļŖö Ļ▓āņ£╝ļĪ£ ļ│┤ņØĖļŗż.
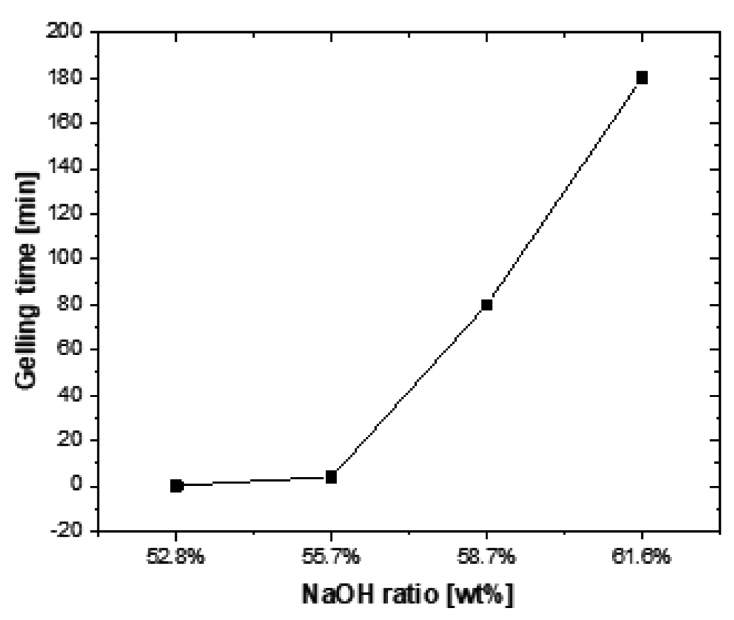
ĻĘĖļ”╝ 9ņØĆ NaOHņØś ļåŹļÅä ļ╣äņ£©ņŚÉ ļö░ļźĖ gelling timeņØä ļ╣äĻĄÉĒĢ£ ĻĘĖļלĒöäļĪ£ NaOHņØś ļåŹļÅäļ╣äĻ░Ć Ļ░Ćņן ļé«ņØĆ 52.8 wt%Ļ░Ć gelling timeņØ┤ 30 secļĪ£ Ļ░Ćņן ņ¦¦ņĢśĻ│Ā ļåŹļÅäļ╣äĻ░Ć Ļ░Ćņן ļåÆņØĆ 61.6 wt%ņØś Ļ▓ĮņÜ░ 180 minņ£╝ļĪ£ Ļ░Ćņן ļŖ”ņØĆ gelling timeņØ┤ ņĖĪņĀĢ ļÉśņŚłļŗż. ĻĘĖļ”¼Ļ│Ā 55.7 wt%ļŖö 4 min, 58.7 wt%ļŖö 80 minņ£╝ļĪ£ ņĖĪņĀĢ ļÉśņŚłļŗż. ZnClņÖĆ NaOHņØś ļåŹļÅäļ╣äĻ░Ć 1:1ņØ┤ ļÉĀņłśļĪØ gelling timeņØĆ ļŖśņ¢┤ļéśļŖö Ļ▓āņ£╝ļĪ£ ĒÖĢņØĖļÉśņŚłļŗż. ļåŹļÅäļ╣ä 52.8 wt%ņÖĆ 55.7 wt%ļŖö Ēü░ ņ░©ņØ┤Ļ░Ć ņŚåņŚłĻ│Ā 58.7 wt% ļČĆĒä░ļŖö gelling timeņØ┤ Ēü¼Ļ▓ī ļŖ”ņ¢┤ņ¦ĆļŖö Ļ▓ĮĒ¢źņØä ĒÖĢņØĖ ĒĢĀ ņłś ņ׳ņŚłļŗż.
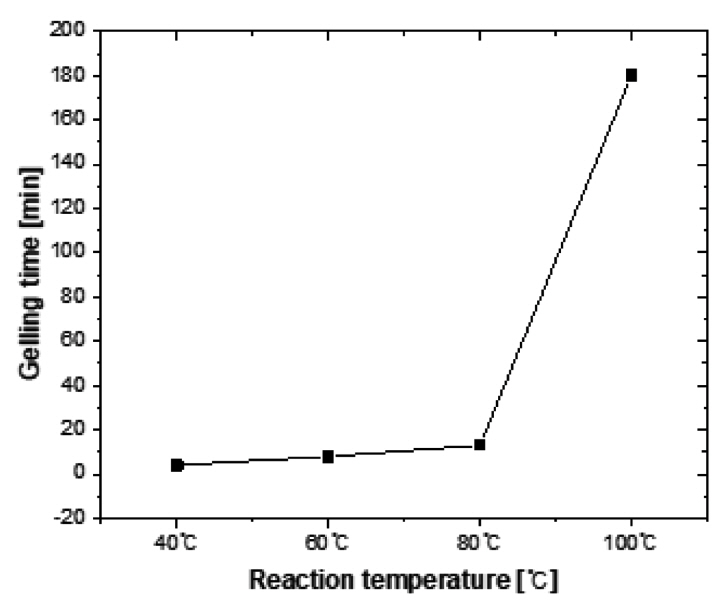
ĻĘĖļ”╝ 10ļŖö ņś©ļÅäņŚÉ ļö░ļźĖ gelling timeņØä ļ╣äĻĄÉĒĢ£ ĻĘĖļלĒöäļĪ£ ņś©ļÅäĻ░Ć 40 ┬░CļĪ£ Ļ░Ćņן ļé«ņØĆ (a)Ļ░Ć 4 minņ£╝ļĪ£ Ļ░Ćņן ņ¦¦ņØĆ gelling timeņØ┤ ļéśņÖöļŗż. 60 ┬░CņØĖ (b)ļŖö 8 min, 80 ┬░CņØĖ (c)ļŖö 13 minļĪ£ Ēü░ ĒÅŁņØś ņ░©ņØ┤ļŖö ņŚåņŚłĻ│Ā 100 ┬░CņØĖ (d)ļŖö 180 minņ£╝ļĪ£ Ēü░ ņ░©ņØ┤ņØś gelling timeņØ┤ ļéśĒāĆļé¼ļŗż.
ĻĘĖļ”╝ 11ņØĆ XRDņĖĪņĀĢņŚÉņä£ ļéśņś© SimonkolleiteĻ▓░ņĀĢĻ│╝ ZnOĻ▓░ņĀĢņØś ļ╣äņ£©ņŚÉ ļö░ļźĖ gelling timeņØä ļ╣äĻĄÉĒĢ£ Ļ▓āņ£╝ļĪ£ SimonkolleiteņØś ļ╣äņ£©ņØ┤ ļåÆņØäņłśļĪØ ņ¦¦ņØĆ gelling timeņØ┤ ļéśņśżļŖö Ļ▓āņØä ĒÖĢņØĖĒĢśņśĆļŗż.
4. Ļ▓░ ļĪĀ
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņ×ÉņÖĖņäĀ ņ░©ļŗ©ņĀ£ņØś ņÜ®ļÅäļĪ£ ņé¼ņÜ®ĒĢśĻĖ░ ņÜ®ņØ┤ĒĢ£ Ļ│ĀĒØĪņ£Ā ĒŖ╣ņä▒ņØä Ļ░¢ļŖö ZnO powder ĒĢ®ņä▒ ļ░Å ĒŖ╣ņä▒ ĒÅēĻ░Ć ļīĆĒĢśņŚ¼ Ļ│Āņ░░ĒĢśņśĆļŗż.
ZnO powderņØś ĒĢ®ņä▒ ņŗ£ NaOH ļ╣äņ£©Ļ│╝ ļ░śņØæ ņŗ£ ņś©ļÅäļź╝ ņĪ░ņĀł ĒĢśņŚ¼ powderņØś Ēü¼ĻĖ░ņÖĆ ĒśĢĒā£ ņĀ£ņ¢┤Ļ░Ć Ļ░ĆļŖźĒĢ©ņØä ĒÖĢņØĖĒĢśņśĆĻ│Ā, XRDļź╝ ĒåĄĒĢ┤ņä£ NaOHņØś ļ╣äņ£©ņØ┤ ļé«ņĢäņ¦ÉņŚÉ ļö░ļØ╝ gelling timeņØ┤ ņżäņ¢┤ļōżņ¦Ćļ¦ī ļ╣äņ£©ņØ┤ 2.79% ļ│┤ļŗż ņżäņ¢┤ļōżļ®┤ ZnOņŚÉ SimonkolleiteĻ░Ć Ēś╝ņ×¼ļÉ£ powderĻ░Ć ĒĢ®ņä▒ļÉśņŚłļŗż. ņØ┤ļ¤¼ĒĢ£ SimonkolleiteĻ░Ć ĒżĒĢ©ļÉ£ ZnOņŚÉņä£ oleic acidļ░śņØæ ņŗ£ Ļ│ĀĒØĪņ£ĀĻ░Ć ņØ╝ņ¢┤ļéśļŖö Ļ▓āņ£╝ļĪ£ ļéśĒāĆļé¼ļŗż.
ļśÉĒĢ£ ļ░śņØæ ņŗ£ ņś©ļÅäĻ░Ć 60 ┬░C ņØ┤ĒĢśļĪ£ ņżäņ¢┤ļōżļ®┤ ZnOņÖĆ SimonkolleiteĻ░Ć Ēś╝ņ×¼ļÉ£ powderĻ░Ć ļ¦īļōżņ¢┤ ņ¦ĆļŖö Ļ▓āņØä ĒÖĢņØĖĒĢśņśĆļŗż. ĻĘĖļ”¼Ļ│Ā ZnO powder 1 ┬Ąm Ēü¼ĻĖ░ņØś ĒīÉņāüņØ┤ ļéśĒāĆļéĀņłśļĪØ ĒØĪņ£ĀĻ░Ć ļåÆņĢäņ¦ĆļŖö Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ļÉ£ļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö Ļ│ĀĒØĪņ£Āļź╝ ņ£äĒĢ£ ZnO ĒĢ®ņä▒ņØä ņłśĒ¢ēĒĢśņśĆĻ│Ā. 40 ┬░C, 60 ┬░CņØś ņś©ļÅäņŚÉņä£ NaOHļ╣äņ£© 52.8 wt%, 55.7 wt%ņŚÉņä£ ņĄ£ņĀüĒÖöļÉ£ ņŖĄņ£ż ĒŖ╣ņä▒ņØä ņ¢╗ņØä ņłś ņ׳ņŚłļŗż.
ĻĖ░ņĪ┤ ZnOņŚÉ ņŚåļŖö ĒØĪņ£Ā ĒŖ╣ņä▒ņØä Ļ░¢ļŖö Ļ▓āņØä gelling time testļź╝ ĒåĄĒĢśņŚ¼ ĒÖĢņØĖ ĒĢśņśĆĻ│Ā XRDļź╝ ĒåĄĒĢ┤ ZnOņØś ĒĢ®ņä▒ņØä ĒÖĢņØĖĒĢśņśĆļŗż.
ļśÉĒĢ£ SEMĻ│╝ XRDļź╝ ĒåĄĒĢśņŚ¼ gelling timeņŚÉ ņśüĒ¢źņØä ļü╝ņ╣śļŖö ņÜöņåīļź╝ ĒÖĢņØĖĒĢśņŚ¼ Ļ▓ĮĒ¢źņä▒ņØä ĒīīņĢģĒĢĀ ņłś ņ׳ņŚłļŗż. gelling timeņØ┤ ņ¦¦ņØĆ Ļ▓ĮņÜ░ Ēü░ ĒīÉņāüņØ┤ ļéśĒāĆļé¼Ļ│Ā SimonkolleiteĻ▓░ņĀĢņØś peakņØ┤ ļéśĒāĆļé£ Ļ▓āņ£╝ļĪ£ ĒÖĢņØĖļÉśņŚłĻ│Ā ņ×æņØĆ ĒīÉņāüĻ│╝ Ļ▓░ņĀĢņä▒ņØ┤ ļåÆņØĆ XRDņØś peakņØ┤ ļéśĒāĆļéĀņłśļĪØ ĻĖ┤ gelling timeņØä Ļ░¢ļŖö Ļ▓āņØä ĒÖĢņØĖĒĢśņśĆļŗż.